Abstract
La spirometria è un test diagnostico cruciale per valutare la funzionalità polmonare, utilizzato per diagnosticare e gestire patologie respiratorie come asma, broncopneumopatia cronica ostruttiva (BPCO), enfisema e fibrosi polmonare. Recenti aggiornamenti delle linee guida dall’American Thoracic Society (ATS) e dalla European Respiratory Society (ERS) hanno sottolineato l’importanza della standardizzazione nella esecuzione e interpretazione della spirometria, al fine di garantire risultati accurati e clinicamente utili.
Spirometry is a crucial diagnostic test for assessing lung function, used to diagnose and manage respiratory conditions such as asthma, chronic obstructive pulmonary disease (COPD), emphysema, and pulmonary fibrosis. Recent updates to the guidelines from the American Thoracic Society (ATS) and the European Respiratory Society (ERS) have emphasized the importance of standardization in the performance and interpretation of spirometry to ensure accurate and clinically useful results.
Introduzione
La spirometria è uno dei test più comuni per valutare la funzionalità polmonare. Viene utilizzata ampiamente per diagnosticare una serie di patologie polmonari, tra cui asma, BPCO, enfisema e fibrosi polmonare. È anche un metodo importante per lo screening e il monitoraggio della salute respiratoria. Durante il test, è fondamentale che il paziente collabori attivamente con il tecnico di spirometria per eseguire correttamente la procedura secondo gli standard stabiliti, garantendo così risultati affidabili per la diagnosi e lo screening. Il personale sanitario coinvolto deve possedere una profonda comprensione della fisiologia e della fisiopatologia polmonare, nonché competenze nell’uso dello spirometro e nella sua manutenzione e verifica. L’obiettivo principale della standardizzazione è ridurre la variabilità determinata da fattori tecnici e umani nel calcolo dei volumi polmonari, consentendo così un’interpretazione accurata e affidabile dei dati, fondamentale per una diagnosi e un trattamento efficaci delle condizioni polmonari (ATA/ERS, 2005).
La standardizzazione della spirometria riveste una grande rilevanza clinica per diversi motivi:
Accuratezza dei risultati diagnostici: Una corretta standardizzazione nella esecuzione e interpretazione della spirometria assicura che i risultati siano accurati e affidabili. Questo è cruciale per una diagnosi precisa delle condizioni respiratorie come l’asma, la BPCO, l’enfisema e la fibrosi polmonare.
Monitoraggio della progressione della malattia: La spirometria è utilizzata non solo per la diagnosi iniziale, ma anche per monitorare nel tempo la funzionalità polmonare dei pazienti con malattie respiratorie croniche. La standardizzazione aiuta a garantire che i cambiamenti nel tempo siano rilevati in modo preciso e sensibile.
Ottimizzazione del trattamento: Con risultati più affidabili e riproducibili, i clinici possono prendere decisioni terapeutiche più informate e personalizzate per i pazienti. Ad esempio, regolare la terapia per il controllo dell’asma o l’ottimizzazione dei farmaci nella gestione della BPCO.
Confrontabilità e coerenza tra studi e centri: La standardizzazione facilita il confronto dei risultati tra studi clinici e tra diversi centri medici. Questo è essenziale per la ricerca clinica e l’analisi epidemiologica delle malattie respiratorie.
Formazione e competenza clinica: Promuovere la standardizzazione attraverso linee guida aggiornate e pratiche consensuali aiuta nella formazione dei professionisti della salute, garantendo che abbiano le competenze necessarie per eseguire e interpretare la spirometria correttamente. Il personale coinvolto deve possedere una profonda comprensione della fisiologia e della fisiopatologia polmonare, nonché competenze nell’uso dello spirometro e nella sua manutenzione e verifica.
In sintesi, la standardizzazione della spirometria non solo migliora la qualità della diagnosi e del monitoraggio delle malattie respiratorie, ma anche la coerenza e la comparabilità dei dati clinici. Ciò porta a miglioramenti significativi nella gestione e nel trattamento delle condizioni polmonari croniche, beneficiando direttamente la salute dei pazienti.
Questa revisione bibliografica sistematica delle linee guida che si concentra sulla letteratura scientifica più recente riguardante la standardizzazione e l’interpretazione della spirometria. Sono state utilizzate banche dati scientifiche come American Journal of Respiratory and Critical Care Medicine e European Respiratory Journal pertinenti per indentificare fonti autorevoli per elaborare una standardizzazione della tecnica di spirometria e di interpretazione.
La ricerca è stata limitata agli articoli pubblicati tra il 2005 e il 2022 che rappresentato le pubblicazioni più recenti e rilevanti sull’argomento. Le parole chiave utilizzate (“spirometria”, “standardizzazione”, “interpretazione”, “linee guida”) sono pertinenti e mirate per identificare studi e documenti che trattano specificamente tecniche di calibrazione, misure di controllo di qualità e protocolli di interpretazione dei risultati.
Le raccomandazioni sono state organizzate secondo le linee guida dell’American Thoracic Society e della European Respiratory Society del 2005 e 2019, nonché le raccomandazioni aggiornate al 2022. Sono stati analizzati ed esclusi studi senza dati specifici sulla standardizzazione della procedura di spirometria, studi non pertinenti alle raccomandazioni dell’ATS e dell’ERS mancanti di misure di controllo di qualità e protocolli di interpretazione dei risultati.
Risultati
L’esecuzione corretta della spirometria richiede la collaborazione attiva del paziente e la competenza del personale sanitario. Durante il test, il paziente deve eseguire una serie di manovre respiratorie, tra cui inspirazione massimale, espirazione forzata e inspirazione a flusso massimale. Queste manovre devono essere eseguite secondo protocolli standardizzati per garantire risultati accurati e riproducibili.
1. Calibrazione dello Spirometro
La calibrazione dello spirometro deve essere effettuata giornalmente, con calibrazione dei flussi utilizzando variazioni di forza pompa diverse ad ogni accensione dell’hardware. Tutti i risultati della spirometria devono essere riportati in condizioni BTPS (Body Temperature, Pressure, Saturated with Water Vapor – temperatura corporea, pressione barometrica ambiente, saturazione di vapore acqueo). La temperatura ambiente deve essere registrata con un’accuratezza di ±1°C. Le variazioni nella temperatura del flussimetro o del sensore di flusso possono essere fonte di variabilità. La temperatura dello spirometro dovrebbe essere misurata e non presumibilmente costante, anche durante una singola sessione di test (ATS/ERS, 2019).
2. Controllo delle Infezioni
È fondamentale eseguire sempre, ad ogni cambio paziente, la disinfezione a freddo secondo le indicazioni fornite dalla casa produttrice dello spirometro. L’obiettivo principale è il controllo delle infezioni, mirando a prevenire la trasmissione di infezioni tra i pazienti e il personale sanitario durante il test. Sebbene il numero di casi documentati di trasmissione di infezioni sia limitato, il potenziale è reale (ATS/ERS, 2019).
3. Preparazione al Test: L’età, l’etnia, il peso e l’altezza del paziente devono essere registrati e misurati accuratamente prima di eseguire la spirometria.
Per la misurazione dell’altezza, il paziente deve essere senza scarpe, con i piedi uniti, mantenendo una postura eretta con gli occhi al livello e lo sguardo diretto davanti a sé, e con la schiena appoggiata contro lo stadiometro. Durante la misurazione, è importante che il paziente rilassi le spalle e tenga la testa secondo il Piano di Francoforte, una linea immaginaria che va dall’orbita inferiore dell’occhio al margine superiore del meato uditivo esterno.
Secondo le linee guida dell’American Thoracic Society/European Respiratory Society (ATS/ERS, 2019) e la Global Lung Function Initiative (GLI), le etnie considerate includono bianco (di ascendenza indoeuropea), afroamericano (nero), asiatico nordorientale, asiatico sudorientale e altro/misto. Le equazioni GLI includono un numero elevato di campioni di individui sani e rappresentano uno standard unico per confrontare le misurazioni osservate applicabili a tutte le età. Servono per stabilire i limiti di normalità specifici per paziente nel test di spirometria (ATA/ERS, 2022). Per prepararsi correttamente al test di spirometria, i pazienti dovrebbero evitare determinate attività, inclusi il fumo un’ora prima del test, il consumo di alcolici nelle 8 ore precedenti, e l’esercizio fisico intenso un’ora prima della prova. Inoltre, è consigliabile evitare di indossare indumenti che limitano l’espansione completa del torace e dell’addome.
È fondamentale fornire al paziente informazioni dettagliate sulla tecnica di spirometria, in modo da ridurre l’ansia che potrebbe influire sull’esito dell’esame e sulla cooperazione del paziente. Le protesi dentarie ben aderenti non influenzano l’esito del test e possono essere mantenute durante la procedura. La decisione di sospendere l’uso di broncodilatatori a lunga e breve durata prima del test dipende dalla finalità dello studio e dalla prescrizione del medico. Se il test è finalizzato a diagnosticare una condizione polmonare, è consigliabile astenersi dall’uso di broncodilatatori prima del test, mentre se lo scopo è valutare la risposta a una terapia già in corso, non è necessario interrompere l’uso di broncodilatatori. Durante il test, il paziente deve essere posizionato su una sedia con braccioli, con la testa leggermente sollevata, indossare il boccaglio e la clip nasale secondo le linee guida dell’American Thoracic Society/European Respiratory Society (ATS/ERS, 2019).
4. Calcolo dei parametri spirometrici
Capacità Vitale (VC): La massima quantità di aria che può essere inspirata ed espirata durante una manovra di respirazione massimale. Questo valore è ottenuto misurando la variazione di volume tra la Capacità Polmonare Totale (TLC) e il Volume Residuo (RV).
Volume Corrente (VC): La quantità di aria inspirata ed espirata in modo normale.
Volume Riserva Inspiratorio (VRi): La massima quantità di aria che può essere ispirata dopo una normale inspirazione.
Volume Riserva Espiratorio (VRe): La massima quantità di aria che può essere espirata dopo una normale espirazione.
Volume Residuo (VR): L’aria intrappolata nei polmoni dopo l’esecuzione di un’espirazione forzata.
Capacità Polmonare Totale (TLC): La somma tra la Capacità Vitale e il Volume Residuo, rappresenta la massima capacità di aria che può essere contenuta nei polmoni (è necessario ridurre il 20 – 25% nelle donne).
Capacità Vitale Forzata (FVC): Il volume d’aria che può essere espirato con uno sforzo massimale dopo che il paziente ha eseguito una massima inspirazione.
Volume Espiratorio Massimo in 1 secondo (FEV1 o VEMS): Il volume d’aria che può essere espirato con uno sforzo massimale in un secondo, dopo che il paziente ha eseguito una piena inspirazione.
Rapporto FEV1/FVC (FEV1% o indice di Tiffeneau): Un indice di ostruzione delle vie aeree. Flusso Espiratorio Forzato (FEF): Il flusso o la velocità con cui l’aria esce dal polmone durante la parte centrale di un’espirazione forzata. Può essere calcolata ad intervalli definiti al 25%, 50% e 75% (FEF 25%, FEF 50%, FEF 75%). Inoltre, può essere misurata la media del flusso durante un intervallo, di solito si calcola la FEF 25-75%.
5. Procedura per la manovra per il calcolo della FVC e FEV1
Per effettuare la manovra occorre distinguere quattro fasi da far eseguire al paziente:
- massima inspirazione,
- espirazione forzata con scatto,
- mantenimento espirazione per un massimo di 15 secondi,
- inspirazione a flusso massimale fino al volume polmonare massimo. Massima inspirazione. Incitare il paziente a eseguire un’unica inspirazione veloce entro i due secondi (2 sec.) e al massimo della sua capacità di riempimento polmonare.
Evitare un’inspirazione lenta o a più riprese in quanto riduce il raggiungimento della Capacità Polmonare Totale (TLC) che riduce il valore della FEV1. Occorre monitorare il paziente che, durante l’esecuzione della manovra, abbia un sollevamento delle sopracciglia e/o la dilatazione degli occhi che sono segni di una massima inspirazione. Un paziente rilassato durante la manovra di inspirazione forzata è un paziente che non ha riempito al massimo i suoi polmoni.
Controllare il display sulla curva volume/tempo per osservare il raggiungimento del plateau respiratorio entro i due secondi (ATS/ERS, 2019). Espirazione forzata. Chiedere al paziente di espellere con scatto e forza tutta l’aria dai polmoni, incoraggiandolo con un feedback specifico. Durante la manovra, monitorare il paziente per segni di sforzo e tensione, come la contrazione dei muscoli toracici e addominali, un’espressione facciale da sforzo e possibili modifiche del colorito cutaneo, come arrossamento.
Nel grafico del display, osservare la curva flusso-volume per verificare la presenza di un istogramma appuntito, che indica una forza adeguata (PEF) nell’espellere l’aria da parte del paziente (ATS/ERS, 2019). Mantenere espirazione forzata. Invitare il paziente a continuare l’espirazione forzata, verificando sul display dello spirometro la durata del Tempo di Espirazione Forzata (FET), che deve essere uguale o superiore a 15 secondi. Durante l’espirazione forzata, osservare eventuali segni di cianosi periferica o stati pre-sincopali. Nei bambini, l’utilizzo di giochi incentivanti nel software dello spirometro può favorire l’esecuzione corretta della manovra. Se il paziente mostra segni di sincope, interrompere immediatamente la manovra forzata.
Alcuni pazienti affetti da malattia polmonare restrittiva o giovani con alta elasticità toracica possono svuotare rapidamente i polmoni e potrebbero non essere in grado di mantenere un plateau espiratorio per 15 secondi (ATS/ERS, 2019). Massima inspirazione dopo un’espirazione forzata. Dopo la completa espirazione forzata occorre incoraggiare il paziente a eseguire una massima inspirazione, espandendo completamente i polmoni.
Questo consente di misurare la Capacità Vitale Inspiratoria Forzata (FIVC), rappresentando uno sforzo massimale per riportare i polmoni alla loro massima capacità dopo l’espirazione forzata. Confrontando la FIVC con la FVC, l’operatore può valutare se il paziente ha iniziato l’espirazione forzata dalla massima espansione. È essenziale incoraggiare l’ispirazione fino alla massima espansione prima e dopo l’espirazione forzata con uguale vigore, garantendo così un confronto valido (ATS/ERS, 2019). Dopo otto manovre è consigliato sospendere l’esame e riprogrammarlo in un secondo momento. Se la FVC o la FEV1 diminuisce del 20%, fermarsi immediatamente e controllare la situazione clinica del paziente. Possibile comparsa di un broncospasmo. (ATA/ERS 2019).
6. Criteri di accettabilità
Una volta eseguita, è fondamentale controllare i criteri di accettabilità della prova. I seguenti criteri sono stati sviluppati come misure oggettive per determinare se è stata effettuata una inspirazione ed espirazione forzata efficace, se sono state ottenute misurazioni accettabili di FEV1 e/o FVC. Tuttavia, in alcuni casi, le manovre che non soddisfano tutti i criteri possono essere il meglio che il paziente è in grado di fare in quell’occasione e, sebbene le misurazioni di FEV1 e/o FVC non siano tecnicamente accettabili, possono essere clinicamente utili cioè “utilizzabili”. Le misurazioni di FEV1 e FVC da una manovra con un volume extrapolato (BEV) > 100ml non sono né accettabili né utilizzabili in quanto comporta un valore erroneamente elevato di FEV1.
I pazienti con ostruzione delle vie aeree nelle alte vie aeree o con malattie neuromuscolari spesso non sono in grado di iniziare rapidamente un aumento del flusso, e il limite di BEV potrebbe essere superiore al limite di accettabilità. Inoltre bisogna occorre aver raggiunto uno dei tre indicatori di fine espirazione forzata (EOFE) che sono: I° criterio: Plateau espiratorio ≤ 0,025 L nell’ultimo secondo dell’espirazione cioè la diminuzione di volume nell’ultimo secondo di espirazione forzata non deve essere superiore a 0,025L. Questo parametro garantisce il completo svuotamento dei polmoni da parte del paziente. II° criterio: Tempo espiratorio (FET) >15 sec. III° criterio: la FVC rientra nella tolleranza di ripetibilità o se è maggiore della più grande FVC osservata in precedenza. In questo caso, il modo di valutare è se il paziente raggiunga ripetutamente lo stesso valore di FVC.
Per l’accettabilità all’interno della manovra, l’FVC deve essere maggiore o entro la tolleranza di ripetibilità del più grande FVC osservato prima di questa manovra nell’insieme di test corrente. Se il volume dell’ispirazione massimale (FIVC) è maggiore di FVC, allora il paziente non ha iniziato la manovra con la Massima Capacità Totale. Le misurazioni di FEV1 e FVC da una manovra con FIVC ≥ FVC + 0,100 L o ≥ 5% di FVC, a seconda di quale sia maggiore, non sono accettabili. Un colpo di tosse durante il primo secondo della manovra può influenzare il valore di FEV1 misurato, e il FEV1 da tale manovra non è né accettabile né utilizzabile.
Tuttavia, il FVC può essere accettabile. La chiusura glottica o il termine anticipato della manovra, come l’ispirazione o il staccarsi dal boccaglio, rende la FVC inaccettabile e se l’espirazione forzata dura meno di un secondo, questo rende il FEV1 inaccettabile e inutilizzabile. L’occlusione del boccaglio (ad esempio, la lingua posta davanti al boccaglio, dai denti davanti al boccaglio o dalla distorsione del boccaglio dovuta al mordere eccessivo se si usa un boccaglio in cartone) può influire sulle prestazioni sia del dispositivo che del paziente (ATS/ERS, 2019).
Fondamentali sono i feedback di correzione forniti per migliorare la tecnica per effettuare una spirometria efficace.
7. Criteri di ripetibilità
Per i pazienti con età maggiore di 6, la differenza tra i due valori FVC più grandi deve essere ≤ 0,150 L; la differenza tra i due valori FEV1 più grandi deve essere ≤ 0,150 L. Per i pazienti con un’età inferiore a 6, la differenza tra i due valori FVC più grandi deve essere ≤ 0,100 L o il 10% del valore più alto; la differenza tra i due valori FEV1 più grandi deve essere ≤ 0,100 L o il 10% del valore più alto.
La tabella n° 1 estrapolata dagli studi ATA/ERS 2019 offrono una sintesi per determinate i criteri di accettabilità e di ripetibilità del paziente adulto e pediatrico.
| Tabella 1 Criteri di accettabilità e ripetibilità della spirometria | ||
| Criteri di accettabilità e utilizzabilità | Requisiti di accettabilità FEV1 FVC | Requisiti di utilizzabilità FEV1 FVC |
| Deve avere un BEV inferiore al 5% di FVC o 0,100 L, a seconda di quale sia il valore maggiore. | SI SI | SI SI |
| Non deve avere tosse nel primo secondo dell’espirazione. Per i bambini di età pari o inferiore a 6 anni, è necessario avere almeno 0,75 secondi di espirazione senza chiusura glottica o tosse per una misurazione accettabile o utilizzabile FEV0,75. | SI NO | SI NO |
| Non deve avere chiusura glottica nel primo secondo dell’espirazione. Per i bambini di età pari o inferiore a 6 anni, è necessario avere almeno 0,75 secondi di espirazione senza chiusura glottica | SI SI | SI SI |
| Non deve avere chiusura glottica dopo 1 s dall’espirazione | NO SI | NO NO |
| Deve raggiungere uno di questi tre indicatori EOFE: Plateau espiratorio (≤0,025 L nell’ultimo sec. dell’espirazione);Tempo espiratorio ≥15 sec.La FVC rientra nella tolleranza di ripetibilità o se è maggiore della più grande FVC osservata in precedenza; la FVC deve essere maggiore o compresa nella tolleranza di ripetibilità della FVC più ampia osservata prima di questa manovra nell’ambito dell’attuale set di test pre-broncodilatatore o post-broncodilatatore. | NO SI | NO NO |
| Non deve esserci evidenza di boccaglio o spirometro ostruito | SI SI | NO NO |
| Non deve esserci alcuna prova di una perdita | SI SI | NO NO |
| Se l’inspirazione massima dopo EOFE è maggiore di FVC, allora la differenza tra FIVC – FVC deve essere ≤ 0,100 L o 5% di FVC. | SI SI | NO NO |
| Criteri di ripetibilità (applicati a valori FVC e FEV1 accettabili) | ||
| Età > 6 anni: la differenza tra i due valori FVC più grandi deve essere ≤ 0,150 L; la differenza tra i due valori FEV1 più grandi deve essere ≤ 0,150 L | ||
| Età ≤ 6 anni: la differenza tra i due valori FVC più grandi deve essere ≤ 0,100 L o il 10% del valore più alto; la differenza tra i due valori FEV1 più grandi deve essere ≤ 0,100 L o il 10% del valore più alto. | ||
| Definizione degli acronimi: BEV volume retro extrapolato; EOFE parte finale dell’espirazione forzata; FIVC inspirazione forzata massima finale | ||
Alcuni pazienti possono non essere in grado di soddisfare i criteri di accettabilità e ripetibilità necessari per la categoria delle linee guida ATS/ERS 2019, ma tuttavia, i loro risultati potrebbero essere clinicamente utili. Ad esempio, la manovra di espirazione forzata può scatenare il riflesso della tosse, e dopo il primo o secondo tentativo, il paziente potrebbe non essere in grado di eseguire un’altra manovra accettabile. In questi casi il giudizio clinico dell’interprete diventa un fattore più importante nell’interpretazione dei risultati. Questo rappresenta un vero cambiamento rispetto alle linee guida ATS/ERS sulla standardizzazione della tecnica della spirometria del 2005. Consente di valutare per i fini clinici anche quelle spirometrie effettuate non con una tecnica soddisfacente (ATS/ERS, 2019).
Feedback correttivi: Fondamentali sono i feedback di correzione forniti per migliorare la tecnica per effettuare una spirometria efficace. I software di nuova generazione forniscono i feedback correttivi che sono sintetizzati nella tabella 2 elaborata dalle linee guide ATS/ERS 2019.
| Tabella 2 Feedback correttivi manovra spirometrica | ||
| Segnale di avviso | Errore commesso | Istruzioni per il paziente |
| BEV supera il limite | inizio esitante | esplodere immediatamente quando i polmoni sono completamente pieni |
| Tempo di riempimento polmonare > 150 ms. Un tempo di riempimento > 150 ms. è spesso associato a uno sforzo espiratorio sub-massimale, caratterizzato da una curva flusso-volume arrotondata, con conseguente FEV1 errato | Riempimento lento | esplodere immediatamente quando i polmoni sono completamente pieni |
| Nessun plateau ed espirazione in < 15 s | No plateau | Continuare ad espirare fino al completo svuotamento dei polmoni |
| Tempo di esitazione > 2 s tra inspirazione ed espirazione forzata | esitazione al massimo volume | esplodere quando si è completamente pieni |
| FVC inferiore alla FVC massima delle manovre precedenti | basso volume espiratorio forzato | fai il respiro più profondo possibile e continua ad andare avanti finché non sei completamente vuoto |
| FIVC > FVC | inspirazione incompleta prima della FVC | riempi completamente i polmoni prima di esplodere: fai il respiro più profondo possibile |
| FIVC < 90%FVC | Inspirazione finale insufficiente | dopo aver svuotato completamente i polmoni, ricordati di inspirare profondamente e completamente a riempire i polmoni al massimo |
| Il flusso inspiratorio prima dell’espirazione forzata è inferiore a 2 L/s | Riempimento lento | inspira più velocemente prima di eseguire espirazione forzata |
| Sospetta chiusura della glottide | arresto brusco | se senti la gola chiudersi, rilassati, ma continua a spingere |
| Sospetta tosse nel primo secondo dell’espirazione | tosse nel primo secondo dell’espirazione | prova a bere un sorso d’acqua prima del prossimo colpo |
| Tempo trascorso dall’ultima manovra pre-broncodilatatore alla prima la manovra post-broncodilatatore è inferiore al tempo di attesa | tempo di attesa del broncodilatatore non rispettato ( > 15 min. post somministrazione) | confermare che il broncodilatatore è stato somministrato e attendere il momento opportuno |
| Verifica della calibrazione accettabile non eseguita il giorno del test | verifica della calibrazione non eseguita nella data del test | eseguire la verifica della calibrazione prima di testare i pazienti |
Capacità Vitale e Capacità Inspiratoria
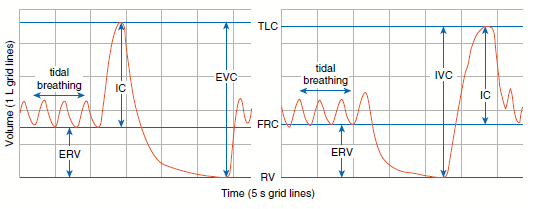
Il valore di Capacità Vitale (VC) nella spirometria rappresenta la massima quantità di aria che un individuo può inspirare ed espirare durante una manovra di respirazione massimale. Questo valore è ottenuto misurando la variazione di volume tra la Capacità Polmonare Totale (TLC) e il Volume Residuo (RV). La VC è un parametro chiave nella valutazione della funzione polmonare e fornisce informazioni sulla capacità polmonare complessiva di una persona. La VC è comunemente suddivisa in due componenti: la Capacità Vitale Inspiratoria (IVC), che rappresenta il volume massimo di aria che può essere inalato lentamente dopo una completa espirazione, e la Capacità Vitale Espiratoria (EVC), che rappresenta il volume massimo di aria che può essere espirato lentamente dopo una completa inspirazione (ATS/ERS, 2019).
La Capacità Inspiratoria (IC) in spirometria rappresenta il massimo volume d’aria che una persona può inspirare lentamente e completamente dopo un’espirazione normale e senza esitazioni. Misura la quantità di aria che può essere inspirata partendo dalla fine di un’espirazione normale (detta Volume Residuale Funzionale, FRC) e raggiungendo la massima espansione polmonare (Capacità Polmonare Totale, TLC).
In termini pratici, la Capacità Inspiratoria fornisce informazioni sulla flessibilità e sulla funzione polmonare di un individuo. È un parametro utile per valutare la capacità polmonare e può essere impiegato per rilevare eventuali restrizioni o alterazioni nella funzione respiratoria. La misurazione della Capacità Inspiratoria è spesso inclusa negli esami spirometrici per ottenere una valutazione completa della capacità respiratoria di un individuo. Procedura del Test Per il calcolo della VC, è preferibile che le manovre siano eseguite prima delle manovre di FVC e FEV1 a causa del potenziale affaticamento muscolare del paziente che può modificare il calcolo dei volumi dopo sforzi inspiratori massimali.
Esecuzione della manovra: una volta che il software calcola tre respiri a volume corrente, invitare il paziente a prendere un respiro profondo fino al massimo della capacità inspiratoria non forzata ed espirare fino ad esaurimento aria nei polmoni con un espirio prolungato per poi riprende aria con un’inspirazione massimale non forzata. Nei pazienti sani, livelli adeguati di inspirazione ed espirazione massimale vengono raggiunti entro 5-6 secondi. Nei pazienti con ostruzione delle vie aeree ci vorrà più tempo, ma l’espirazione dovrebbe essere interrotta dopo 15 secondi.
L’espirazione non dovrebbe essere eccessivamente lenta, poiché ciò può portare a una sottostima della capacità vitale. Occorre osservare attentamente il paziente per assicurarsi che le labbra siano sigillate intorno al boccaglio, che nulla ostruisca il boccaglio, la clip nasale ben posizionata e senza perdite d’aria dal naso e che la TLC e RV siano raggiunti. La capacità inspiratoria può essere sottostimata se la manovra inspiratoria è troppo lenta a causa di uno sforzo insufficiente o di esitazioni o se c’è una chiusura prematura delle corde vocali. Eseguita questa manovra occorre far respirare normalmente il paziente e senza staccare il paziente dal boccaglio, prepararlo alla respirazione profonda continuata per il washout dell’azoto per il calcolo del Volume Residuo.
Il Washout dell’Azoto è una procedura utilizzata per misurare il volume polmonare residuo (RV) attraverso l’uso di una miscela di gas contenente azoto. Questo tipo di test è comunemente noto come la diluizione dell’azoto e viene eseguito utilizzando un dispositivo di diluizione che mescola una piccola quantità di gas contenente azoto con l’aria inspirata dal paziente.
Viene eseguita attraverso i seguenti passaggi:
1) il paziente inizia a respirare una miscela di gas contenente azoto attraverso il boccaglio collegato a un dispositivo di misurazione dei gas.
2) durante la respirazione del paziente, il concentrato di azoto espirato viene continuamente misurato per determinare quanto azoto è presente nel polmone.
3) conoscendo la concentrazione iniziale di azoto nella miscela e monitorando la sua diminuzione nel tempo, è possibile calcolare il volume polmonare residuo del paziente (ATS/ERS, 2019).
La figura 1 descrive la tecnica esecutiva. Questo test è particolarmente utile nella valutazione di condizioni come l’ostruzione delle vie aeree e nei pazienti con malattie polmonari restrittive. Per la valutazione tra le manovre, come per le manovre forzate, è necessario ottenere un minimo di tre manovre di VC accettabili. Se la differenza nella VC tra la manovra più grande e la successiva più grande è di almeno 0,150L o il 10% della VC, a seconda di quale sia più piccolo, per i pazienti di età superiore ai 6 anni o di almeno 0,100 L o il 10% della VC, a seconda di quale sia più piccolo, per quelli di età inferiore ai 6 anni, allora dovrebbero essere effettuate prove aggiuntive.
Per soddisfare i criteri di ripetibilità potrebbe essere necessario eseguire fino a otto manovre, con un sufficiente periodo di riposo tra le manovre in modo che l’operatore e il paziente concordino che la successiva manovra possa iniziare. Una grande variabilità in questo test è spesso dovuta a un’inspirazione incompleta (ATA/ERS, 2019).
Figura 1. Misurazione della Capacità Vitale (VC) e della Capacità Inspiratoria (IC). La VC può essere misurato sia come EVC (pannello sinistro) che come IVC (pannello destro). In questi esempi, le divisioni sull’asse del volume sono di 1 L, e quelle sull’asse del tempo sono di 5 secondi. ERV = Volume di Riserva Espiratoria; EVC = Capacità Vitale Espiratoria; IC = Capacità Inspiratoria; IVC = Capacità Vitale Inspiratoria; RV = Volume Residuo.
Interpretazione dei risultati secondo linee guida ATS/ERS 2022
I limiti di normalità rappresentano i valori del 5° e del 95° percentile (-1.645 e +1.645 z-score) della popolazione sana e possono essere utilizzati per identificare individui con risultati insolitamente bassi o alti, rispettivamente. L’equazione dello z-score si riferisce a quello misurato dalla Global Lung Function Initiative (GLI) per il calcolo dei volumi statici e dinamici per definire l’intervallo dei valori attesi in individui sani. Le equazioni GLI includono un numero elevato di campioni di individui sani e rappresentano uno standard unico per confrontare le misurazioni osservate applicabili a tutte le età e etnie.
Un intervallo di riferimento rappresenta la distribuzione dei valori che ci si aspetta in una popolazione sana e il limite inferiore di normalità (LLN) rappresenta una soglia per definire risultati al di fuori del range di valori tipicamente osservati in condizioni di salute. Gli z-scores o i valori percentile definiti dalla popolazione descrivono la probabilità che il risultato osservato cada all’interno della distribuzione di valori in individui sani (figura 2).
Figura 2: Distribuzione normale con punteggi Z e percentili visualizzati. Il percentile può essere interpretato come la probabilità che un individuo sano ottenga risultati compresi nell’intervallo normale.
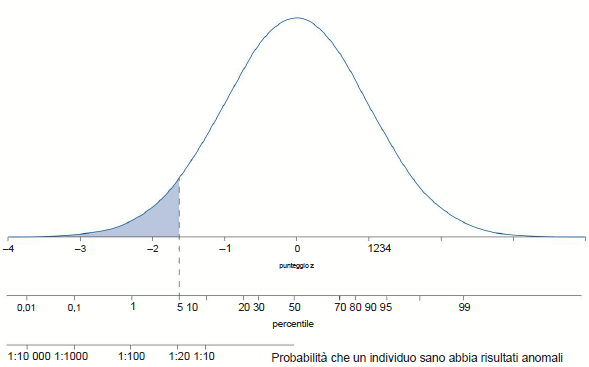
Dovrebbe essere utilizzato un sistema a tre livelli per valutare la gravità del deterioramento della funzione polmonare utilizzando i valori dello z-score; gli z-score > -1,645 sono considerati normali, quelli compresi tra -1,65 e -2,5 sono considerati lievi, quelli compresi tra -2,51 e -4 sono moderati e quelli inferiori a -4,1 sono considerati gravi. La magnitudine della deviazione della funzione polmonare rispetto a quanto ci si aspetta in individui sani, tenendo conto della variabilità legata all’età. I livelli degli z-score tra -1,65 e -2,5 hanno una differenza minima nel rischio di mortalità e sono stati quindi uniti in un gruppo “lieve”. Gli individui con z-score tra -2,51 e -4 presentano un rischio moderato di mortalità e queste categorie sono state quindi unite nella categoria chiamata “moderato”. Gli individui con uno z-score superiore a -4 presentano un rischio “severo” di mortalità (ATS/ERS, 2022).
Un riassunto delle modifiche rispetto allo standard di interpretazione del 2005 può essere trovato nella tabella 3.
| Tabella 3. Sommario delle differenze tra gli standard di interpretazione della American Thoracic Society (ATS) e della European Respiratory Society (ERS) del 2005 e del 2021 2005 ATS/ERS 2021 ATS/ERS | ||
| Approccio generale | L’accento era sull’utilizzo dell’interpretazione delle prove di funzione polmonare (PFT) per assistere nella diagnosi clinica e nelle decisioni | Vi è una maggiore enfasi sull’utilizzo delle PFT per classificare la fisiologia, piuttosto che per fare una diagnosi clinica. Si pone maggior attenzione sull’incertezza dell’interpretazione, specialmente vicino al limite inferiore della norma (LLN). |
| Equazione di riferimento | Preferenza per l’uso di equazioni specifiche per razza/etnia piuttosto che l’utilizzo di fattori di correzione. Spirometria: Negli Stati Uniti: consigliato NHANES III. In Europa: nessuna equazione specifica raccomandata Volumi polmonari e DLCO: Negli Stati Uniti e in Europa: nessuna equazione specifica raccomandata | Raccomandazione di utilizzare le equazioni di riferimento GLI per spirometria, volumi polmonari e DLCO. Maggiore enfasi sull’incompleta comprensione del ruolo di razza/etnia sulla funzione polmonare. Chiarire che il sesso biologico, non il genere, debba essere utilizzato per interpretare la funzione polmonare. |
| Definizione dell’intervallo normale | • Uso generale di LLN=5° percentile • Sconsigliato l’uso del rapporto fisso FEV1/FVC <0,7 • Sconsigliato l’uso del 80% previsto per definire il normale | • Uso generale di LLN=5° percentile e ULN=95° percentile • Sconsigliato l’uso del rapporto fisso FEV1/FVC <0,7 • Sconsigliato l’uso del 80% previsto per definire il normale |
| Risposta test di broncodilatazione | • ≥12% e 200 mL in FEV1 o FVC rispetto al valore iniziale • 4 dosi di 100 μg di salbutamolo; attesa di 15 minuti | • >10% del valore previsto in FEV1 o FVC • La scelta del protocollo per somministrare il broncodilatatore non è specificata |
| Interpretazione dei cambiamenti nel tempo | Cambiamenti variabili nel tempo a seconda della normalità rispetto alla BPCO e del periodo temporale (all’interno di un giorno, da una settimana all’altra, da un anno all’altro). | • Punteggio di cambiamento condizionale nei bambini • FEV1Q negli adulti |
| Gravità dell’alterazione della funzione polmonare | • Utilizzo di FEV1 (include ostruzione o restrizione): Lieve: FEV1 >70% previsto Moderata: 60–69% previsto Moderata-grave: 50–59% previsto Grave: 35–49% previsto Molto grave: <35% previsto • DLCO: Lieve: >60% previsto e <LLN Moderata: 40−60% previsto Grave: <40% previsto | • Per tutte le misure utilizzare lo z-score: – Lieve: da −1,65 a −2,5 Moderata: da −2,51 a −4,0 Grave: <−4,1 |
| Classificazione delle compromissioni fisiologiche | • Ostruzione del flusso d’aria: FEV1/FVC <5° percentile, utilizzando il VC più grande; volumi polmonari per rilevare l’iperinflazione o il blocco dell’aria; resistenza delle vie aeree elevata; ostruzione delle vie aeree centrali/superiori • Restrizione: TLC <5° percentile e FEV1/VC normali, Mista: FEV1/VC e TLC <5° percentile | • Ostruzione del flusso d’aria: FEV1/FVC <5° percentile, utilizzando l’FVC; Questa definizione indica che l’ostruzione del flusso d’aria è presente quando il rapporto FEV1/FVC è inferiore al 5° percentile, e l’FVC viene utilizzato per confermare tale ostruzione. Inoltre, si fa riferimento all’uso dei volumi polmonari per identificare l’iperinflazione o il blocco dell’aria, alla presenza di dysanapsis (uno squilibrio nello sviluppo delle vie aeree), a un pattern non specifico e a PRISm (preserved ratio impaired spirometry), oltre a menzionare l’ostacolo nelle vie aeree centrali o superiori. • Restrizione: TLC <5° percentile Restrizione semplice versus complessa Iperinflazione Mista |
Conclusioni
Questa revisione scientifica della letteratura basata sulla standardizzazione della spirometria secondo le linee guida dell’American Thoracic Society (ATS) e dell’European Respiratory Society (ERS) del 2019, nonché sull’interpretazione dei risultati basata sulle più recenti linee guida del 2022, indica una crescente adozione e implementazione di queste linee guida da parte dei professionisti sanitari nel contesto della diagnosi e gestione delle patologie polmonari.
Le evidenze disponibili supportano l’importanza della corretta esecuzione della spirometria e della sua interpretazione accurata per una valutazione clinica efficace e una gestione ottimale dei pazienti affetti da malattie polmonari. L’interpretazione dei risultati della spirometria basato sull’equazione dei GLI 2012 permette una refertazione molto più personalizzata rispetto alle altre metodiche di refertazioni che si basano su canoni rigidi e non personalizzati. L’andamento dell’American Thoracic Society e dell’European Respiratory Society è quello di implementare studi mirati a rendere l’interpretazione dei dati della spirometria i più personalizzati possibili.
Bibliografia
1. Miller, M.R., Hankinson, J., Brusasco, V., et al. (2005). Standardisation of spirometry. **European Respiratory Journal**, 26(2), 319-338.
2. Pellegrino, R., Viegi, G., Brusasco, V., et al. (2005). Interpretative strategies for lung function tests. **European Respiratory Journal**, 26(5), 948-968.
3. Graham, B.L., Steenbruggen, I., Miller, M.R., et al. (2019). Standardization of Spirometry 2019 Update. **An official American Thoracic Society and European Respiratory Society Technical Statement**. *American Journal of Respiratory and Critical Care Medicine*, 200(8), e70-e88.
4. Global Lung Function Initiative (GLI). (2022). **GLI Spirometry reference values**. [GLI Network] (https://www.ers-education.org/guidelines/global-lung-function-initiative.aspx).
5. American Thoracic Society (ATS). (2019). Pulmonary Function Laboratory Management and Procedure Manual. **ATS Publications**.
6. Stanojevic, S., Kaminsky, D.A., Miller, M.R., et al. (2021). ERS/ATS technical standard on interpretive strategies for routine lung function tests. **European Respiratory Journal**, 60(1), 2101499.
Autori
dott. Marco Gallifuoco, infermiere del Servizio di Allergologia ambulatorio di fisiopatologia respiratoria dell’Azienda Ospedaliero Universitaria delle Marche
dott. Francesco Scuro, infermiere del reparto di Direzione Medica Ospedaliera dell’Azienda Ospedaliero Universitaria della Marche
Leggi anche:
- La spirometria: cos’è e a cosa serve
- Fibrosi polmonare: tutto quello che c’è da sapere
- Allergie, per scovarle non basta più il test cutaneo: va scoperta nel sangue la molecola scatanente
- Intramoenia: i dati del Report Agenas su tempi di attesa e volumi delle prestazioni libero-professionali (anno 2021)
- Long Covid, nata la prima associazione di pazienti che lo hanno sconfitto
Scopri come guadagnare pubblicando la tua tesi di laurea su NurseTimes
Il progetto NEXT si rinnova e diventa NEXT 2.0: pubblichiamo i questionari e le vostre tesi
Carica la tua tesi di laurea: tesi.nursetimes.org
Carica il tuo questionario: https://tesi.nursetimes.org/questionari










Lascia un commento