Alla maggior parte dei pazienti ocorre un acceso venoso periferico (generalmente un catetere endovenoso periferico) nel corso della propria degenza in ospedale.
Un dispositivo si rende necessario per la somministrazione di liquidi e farmaci, trasfusioni ematiche o nutrizione parenterale.
Le complicazioni di un CVP sono frequenti ma è possibile prevenirle o ridurle effettuando una valutazione frequente e routinaria dello stesso. L’articolo analizza gli aspetti principali della valutazione di un CVP.
Un CVP è davvero necessario?
Il paziente ha veramente bisogno di un CVP?
Molti CVP vengono lasciati in sede anche quando il paziente non ha terapie infusive o farmaci endovenosi in corso (Limm et al. 2013; New et al. 2014).
Ad alcuni pazienti vengono posizionati due, tre o più CVP contemporaneamente, nonostante sarebbe sufficiente averne a disposizione uno solo nella maggior parte dei casi (New et al., 2014). Esistono addirittura reports di pazienti dimessi a domicilio con un CVP posizionato perché nessuno dei professionisti sanitari si è ricordato di rimuoverlo. (TracyVaRN 2011).
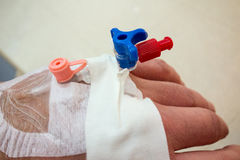
I CVP sono spesso lasciati posizionati “in caso di necessità” del paziente. Ma ogni cannula si immette direttamente nel torrente ematico e può essere fonte di infezione. (Zingg & Pittet, 2009).
La valutazione del bisogno di mantenere posizionato un CVP dovrebbe essere valutato ad ogni turno. Qualora non sis stato utilizzato nelle ultime 24 ore oppure non si prevede di doverlo utilizzare nelle prossime 24 ore, dovrebbe essere rimosso.
Alcune eccezioni possono verificarsi in caso di procedure invasive pianificate, monitoraggio cardiaco, paziente con precedente storia clinica convulsiva, pazienti in condizioni instabili o che sono stati sottoposti a recenti interventi farmacologici o infusivi urgenti.
Il CVP funziona correttamente?
Quando un CVP è posizionato, un reflusso di sangue nella camera conferma il corretto posizionamento in vena. Successivamente, il posizionamento della cannula viene valutando verificando il flusso della soluzione endovenosa infusa (a caduta o tramite pompa infusionale) o mediante lavaggio endovenoso (tecnica iniettiva manuale).
Praticare un lavaggio del CVP con soluzione NaCl 0,9% prima e dopo una somministrazione ebdivenosa riduce il rischio di miscelazione di più farmaci riducendo il rischio di occlusione. (Goossens 2015).
I CVP spesso si occludono, si inginocchiano o si dislocano, pertanto è necessario assicurarsi che funzionino prima di ogni utilizzo non ravvicinato nel tempo.
È possibile valutare la funzionalità del CVP ponendosi due semplici domande:
- È possibile effettuare un lavaggio senza percepire particolari resistenze?
- La soluzione infusionale incontra particolari resistenze durante l’infusione? (Flusso rallentato)
Resistenze o impossibilità ad effettuare il lavaggio o l’infusione indicano che il CVP potrebbe essere inginocchiato, ostruito o potrebbe essersi dislocato fuori dalla vaso sanguigno (INS 2016; Goossens 2015).
Il paziente tollera il CVP?
È opportuno fornire spiegazione esaustive riguardanti la necessità di posizionare il dispositivo per un determinato trattamento verificando la comprensione del messaggio trasmesso al paziente e ai famigliari. È bene invitare gli interlocutori a riferire qualsiasi problema quale dolore localizzato, fuoriuscita di liquido, gonfiore, etc.
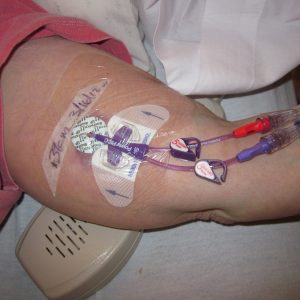
Il CVP correttamente posizionato non dovrebbe provocare dolore al paziente. Il sintomo riferito potrebbe essere un prodromo di flebite e deve far sospettare un disfunzionento del catere che dovrà essere rimosso. (Ray-Barruel et al., 2014). Qualora il paziente avesse ancora bisogno di infusioni e le vene fossero particolarmente fragili, sara opportuno considerare l’inserimento di un dispositivo differente, come un PICC (Chopra et al. 2015; Moureau et al. 2012).
Uno studio irlandese ha dimostrato che i pazienti fossero sette volte più propensi a mantere un PICC inutilizzato, quando ignari del motivo per il quale fosse posizionato (McHugh et al., 2011).
Coinvolgere il paziente ed i famigliari permette loro di esternare dubbi ed incertezze, permettendo all’Infermiere di gestire eventuali problematiche e di considerare la rimozione del PICC.
La Cannula è correttamente ancorata?
Cerotti trasparenti in poliuretano o garze sterili e cerotto in tessuto non tessuto sono entrambi raccomandati (Marsh et al. 2015). I cerotti in poliuretano sono più convenienti, poiché garantiscono la visibilità del sito di inserzione e possono rimanere in sede per 7 giorni. Ancoraggio con garza e cerotto sono più funzionali in caso di pazienti diaforetici, ma devono essere sostituiti ogni 2 giorni.
Le medicazioni devono presentarsi pulite, asciutte ed intatte per prevenire una contaminazione microbica del sito. È opportuno sostituire la medicazione del PICC qualora diventi umida, visibilmente sporca o non più aderente assicurando l’estremita distale ed eventuali deflussori per infusione con cerotto in tessuto non tessuto o bendaggio, lasciando il sito visibile (INS 2016).

Gli audit ospedalieri dimostrano come il 25% delle medicazioni dei PICC non siano pulite, asciutte e inyatte (New et al. 2014; Alexandrou et al. 2015).
Ciò aumenta il rischio di infezione e di dislocamento della cannula. Un PICC non ancorato correttamente può essere causa di infezione, poiché il movimento della cannula in vena può favorire la migrazione di microrganismi lungo la stessa permettendo il raggiungimento del torrente ematico (Marsh et al, 2015).
Sono presenti Segni di Infezione?
I PICC sono frequentemente utilizzati e spesso si sottovalutano i rischi di infezione.
Questi possono essere ridotto notevolmente attraverso una rigida igiene delle mani prima e dopo qualsiasi manovra sul dispositivo, sulla medicazione o su linee infusionali o connettori.
Una tecnica asettica non-touch è essenziale durante la procedura di connessione delle linee (INS, 2016). I connettori needleless dovrebbero essere disinfettati per 15 secondi attendendo successivamente che asciughino prima del loro utilizzo. (Moureau & Flynn, 2015).
È opportuno non trascurare la possibilità di infezioni sistemiche. Qualora il paziente manifesti sintomi specifici (ipo o ipertermia, tachicardia, tachipnea, ipoleucocitosi o iperleucocitosi), ogni dispositivo dovrebbe essere considerato come possibile causa. (Shah et al. 2013), ed i siti di inserzione andrebbero esaminati in cerca di segni di infezione o suppurazione. Se un paziente dovesse manifestare segni di infezione senza una motivazione oggettiva, è opportuno considerare la rimozione del PICC.
Come possono i batteri raggiungere il torrente ematico?
Quali altre complicazioni sono possibili?
Sfortunatamente, circa il 40% dei PICC presenta complicazioni, si ostruisce, o si disloca prima che il ciclo terapeutico prescritto sia concluso (Wallis et al. 2014).
Complicanze riguardanti il PICC spesso si traducono in dolore e dispendio di tempo per sostituire il dispositivo che, spesso può risultare complesso, soprattutto in caso di pazienti pediatrici, anziani, e in coloro che dispongano di scarso patrimonio venoso.
Molti ospedali utilizzano scale di valutazione delle flebiti per migliorare la valutazione dei PICC. Le scale di valutazione delle flebiti non sono strumenti considerati validi dal punto di vista scientifico e pertanto non sono raccomandati (Ray-Barruel et al., 2014).
Mentre le flebiti sono motivo di preoccupazione, il non funzionamento del catere venoso è più frequentemente causativo da occlusioni, infiltrazioni o dislocazione accidentale (Wallis et al., 2014).
Complicanze del CVP più frequenti:
Le flebiti sono caratterizzate da almeno una di queste caratteristiche: dolore, eritema, gonfiore, calore, arrossamento lungo il tratto venoso, turgore del sito di inserzione o prurito.
Per infiltrazione si intende la fuoriuscita di una soluzione non vescicante nei tessuti adiacenti ai vasi sanguigni, causando dolore e gonfiore.
Per stravaso si intende la migrazione nei tessuti di un farmaco o soluzione vescicante, quali un chemioterapico. Ciò può essere molto doloroso e causare traumi tissutali maggiori.
Per trombosi o tromboflebite si intende la formazione di un coagulo nel vaso sanguigno, spesso causato dal movimento della cannula all’interno del vaso sanguigno, con rischio di danneggimanto della parete vascolare.
Durante l’inserzione di un PICC potrebbero verificarsi lesioni nervose. Se il paziente dovesse riferire un dolore pungente localizzato al braccio, o parestesie dell’estremità, la cannula dovrà essere rimossa immediatamente.
Un dislocamento partiale o completo del PICC può indicare che il dispositivo non sia più in vena, pertanto sarà necessario rimuoverlo. Il riconoscimento ed il trattamento precoce delle complicazioni può prevenire complicanze a lungo termine.
Qualora si sospettino infiltrazione o stavaso, sarà necessario interrompere immediatamente l’infusione, disconnettendo il deflussore e tentato di aspirare i residui di farmaco dal device.
Qualora il sito di inserzione presenti iperemia, gonfiore o dolore, sarà necessario posizionare l’arto in scarico, consultare un medico, e posizionare impacchi caldo o freddi, a seconda della tollerabilità del paziente. (Doellman et al., 2009).
Il dolore può essere trattato farmacologicamtne con il paracetamolo, qualora non sia controindicato. Sarà necessario rivalutare regolarmente il paziente, documentando le proprie valutazioni ed azioni intraprese, oltre alla risposta del paziente.
In conclusione, è necessario ricordare che una flebite post-infusionale potrebbe manifestarsi anche 48 ore dopo l’avvenuta rimozione del PICC (Webster et al., 2015), pertanto sara importante valutare anche i precedenti siti di inserzione di cateteri venosi, proprio come i siti attuali.
Simone Gussoni
Bibliografia:
- Alexandrou, E, Ray-Barruel, G, Carr, PJ, Frost, S, Inwood, S, Higgins, N, Lin, F, Alberto, L, Mermel, L & Rickard, CM 2015, ‘International prevalence of the use of peripheral intravenous catheters’, Journal of Hospital Medicine, vol. 10, no. 8, pp. 530-3, https://www.ncbi.nlm.nih.gov/pubmed/26041384
- TracyVaRN 2011,’Has anyone ever discharged a patient with their IV still in?’, posted in Allnurses.com, viewed 27 March 2017, https://allnurses.com/general-nursing-discussion/has-anyone-ever-578675.html
- Chopra, V, Flanders, SA, Saint, S, Woller, SC, O’Grady, NP, Safdar, N, Trerotola, SO, Saran, R, Moureau, N, Wiseman, S, Pittiruti, M, Akl, EA, Lee, AY, Courey, A, Swaminathan, L, LeDonne, J, Becker, C, Krein, SL, & Bernstein, SJ 2015, ‘The Michigan Appropriateness Guide for Intravenous Catheters (MAGIC)’, Annals of Internal Medicine, vol. 163, no. 6, viewed 27 March 2017, https://www.teleflex.com/anz/australia-education/clinical-resources/Chopra15MAGICGuidelines.pdf
Doellman, D, Hadaway, L, Bowe-Geddes, - LA, Franklin, M, LeDonne, J, Papke-O’Donnell, L, Pettit, J, Schulmeister, L & Stranz, M 2009, ‘Infiltration and extravasation: update on prevention and management’, Journal of Infusion Nursing, vol. 32, no. 4., pp. 203-11, viewed 27 March 2017, https://www.ncbi.nlm.nih.gov/pubmed/19605999
- Goossens, GA 2015, ‘Flushing and locking of venous catheters: available evidence and evidence deficit’, Nursing Research and Practice, 2015, viewed 27 March 2017, https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4446496/
- Infusion Nurses Society 2006, ‘Infusion therapy standards of practice’, Journal of Infusion Nursing, supp. 1
- Limm, EI, Fang, X, Dendle, C, Stuart, R& Egerton Warburton, D 2013, ‘Half of all peripheral intravenous lines in an Australian tertiary emergency department are unused: Pain with no gain?’, Annals of Emergency Medicine, vol. 62, no. 5, pp. 521-5, viewed 27 March 2017, https://www.ncbi.nlm.nih.gov/pubmed/23623052
- Marsh, N, Webster, J, Mihala, G & Rickard, CM 2015, ‘Devices and dressings to secure peripheral venous catheters to prevent complications’, The Cochrane Database of Systematic Reviews, vol. 12, no. 6, viewed 27 March 2017, https://www.ncbi.nlm.nih.gov/pubmed/26068958
- McHugh, SM, Corrigan, MA, Dimitrov, BD, Morris-Downes, M, Fitzpatrick, F, Cowman S, Tierney, S, Hill, AD & Humphreys, H, ‘Role of patient awareness in prevention of peripheral vascular catheter-related bloodstream infection’, Infect Control and Hospital Epdemiology, vol. 32, no. 1, pp. 95-6, viewed 27 March 2017, https://www.ncbi.nlm.nih.gov/pubmed/21087126
- Moureau, NL, Trick, N, Nifong, T, Perry, C, Kelley, C, Carrico, R, Leavitt, M, Gordon, SM, Wallace, J, Harvill, M, Biggar, C, Doll, M, Papke, L, Benton, L & Phelan, DA 2012, ‘Vessel health and preservation (Part 1): A new evidence-based approach to vascular access selection and management,’ The Journal of Vascular Access, vol. 13, no. 3, pp. 351-6, viewed 27 March 2017, https://www.vascular-access.info/article/vessel-health-and-preservation-part-1–a-new-evidence-based-approach-to-vascular-access-selection-and-management
- Moureau, NL & Flynn, J 2015, ‘Disinfection of needleless connector hubs: Clinical Evidence Systematic Review,’ Nursing Research and Practice, vol. 2015, viewed 27 March 2017, https://www.hindawi.com/journals/nrp/2015/796762/
- New, KA, Webster, J, Marsh, NM & Hewer, B 2014, ‘Intravascular device use, management, documentation and complications: a point prevalence survey’, Australian Health Review, vol. 38, no. 3, pp. 345-9, viewed 27 March 2017, https://www.ncbi.nlm.nih.gov/pubmed/24869909
- Ray-Barruel, G, Polit, DF, Murfield, JE & Rickard, CM 2014, ‘Infusion phlebitis assessment measures: a systematic review’, Journal of Evaluation in Clinical Practice, vol. 20, no. 2, pp. 191-202, viewed 27 March 2017, https://www.ncbi.nlm.nih.gov/pubmed/24401116
- Shah, H, Bosch, W, Thompson, KM & Hellinger, WC 2013, ‘Intravascular catheter-related bloodstream infection’, Neurohospitalist, vol. 3, no. 3, pp. 144-51, viewed 27 March 2017, https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3805442/
- Wallis, MC, McGrail, M, Webster, J, Marsh, N, Gowardman, J, Playford, G, Rickard, CM 2014, ‘Risk factors for peripheral intravenous catheter failure: a multivariate analysis of data from a randomized controlled trial’, Infection Control and Hospital Epidemiology, vol. 35, no. 1, pp. 63-8, viewed 27 March 2017, https://www98.griffith.edu.au/dspace/bitstream/handle/10072/61124/91756_1.pd
- Webster, J, McGrail, M, Marsh, N, Wallis, MC, Ray-Barruel, G & Rickard, CM 2015, ‘Postinfusion phlebitis: incidence and risk factors’, Nursing Research and Practice, vol. 2015, viewed 27 March 2017, https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4446485/
- Zingg, W & Pittet, D 2009, ‘Peripheralvenous catheters: an under-evaluated problem’, International Journal of Antimicrobial Agents, vol. 34, supp. 4, viewed 27 March 2017, https://www.ncbi.nlm.nih.gov/pubmed/19931816











Lascia un commento