Secondo la definizione della IASP (International Association for the Study of Pain – 1986) e secondo l’O.M.S. il dolore è “un’esperienza sensoriale ed emozionale spiacevole associata a danno tissutale, in atto o potenziale, o descritta in termini di danno”.
Esso non può essere descritto veramente come un fenomeno sensoriale, bensì deve essere visto come la composizione di una parte percettiva (la nocicezione) che costituisce la modalità sensoriale che permette la ricezione ed il trasporto al sistema nervoso centrale di stimoli potenzialmente lesivi per l‟organismo, e di una parte esperienziale (quindi del tutto privata, la vera e propria esperienza del dolore) che è lo stato psichico collegato alla percezione di una sensazione spiacevole.
L’esperienza del dolore è quindi determinata dalla dimensione affettiva e cognitiva, dalle esperienze passate, dalla struttura psichica e da fattori socio-culturali. Il dolore è fisiologico, un sintomo vitale/esistenziale, un sistema di difesa, quando rappresenta un segnale d’allarme per una lesione tissutale, essenziale per evitare un danno; diventa patologico quando si automantiene, perdendo il significato iniziale e diventando a sua volta una malattia (sindrome dolorosa cronica).
Dal punto di vista della durata temporale, il dolore è classificabile come:
- Transitorio: vi è attivazione dei nocicettori, corpuscoli responsabili della trasmissione degli stimoli dolorosi, senza danno tissutale. Scompare con la cessazione dello stimolo.
- Acuto: è un dolore nocicettivo, di breve durata in cui solitamente il rapporto di causa/effetto è evidente: nel dolore acuto, per effetto di una causa esterna o interna, si ha una fisiologica attivazione dei nocicettori. Si ha, in genere, un danno tissutale; il dolore scompare con la riparazione del danno.
- Recidivo: come spesso si ha in pazienti con cefalea.
- Persistente: la permanenza dello stimolo nocicettivo o della nocicezione rendono il dolore “persistente”.
- Cronico: dolore associato a profonde modificazioni della personalità e dello stile di vita del paziente che costituiscono fattori di mantenimento indipendenti dall’azione dei nocicettori.
Il dolore può avere due accezioni: utile e non utile. Diventa utile quando esso rappresenta un campanello d’allarme e ci fa capire che siamo di fronte a un potenziale problema più o meno grave. Tutti i dolori che non fanno le veci di un campanello d’allarme sono inutili e devono essere soppressi; tali dolori sono rappresentati da tutti i tipi di dolore cronici, di qualunque natura essi siano, sia benigni che maligni.
Dal punto di vista eziologico il dolore si può distinguere in:
- dolore nocicettivo basato primordialmente sull’irritazione dei sensori di dolore (nocicettori) e trasmissione degli impulsi (trasmissione di dolore) al sistema nervoso centrale;
- dolore neuropatico in seguito a lesioni del sistema nervoso periferico o del sistema nervoso centrale (es. dopo amputazione, paraplegia, infezioni da herpes, polineuropatia diabetica);
- dolore funzionale in seguito a disturbi funzionali come: mal di schiena causato da impostura e movimenti abitudinali disfunzionali; meccanismi psicosomatici e riflessivi vegetativi
- dolore misto : associazione di dolore nocicettivo e neuropatico.
In tutto ciò, l’OMS ha delineato, nel 1986, la scala analgesica a grandi gradini, che permette d’impostare il trattamento farmacologico del dolore e classifica in tre step i farmaci analgesici sulla base della loro potenza antidolorifica.
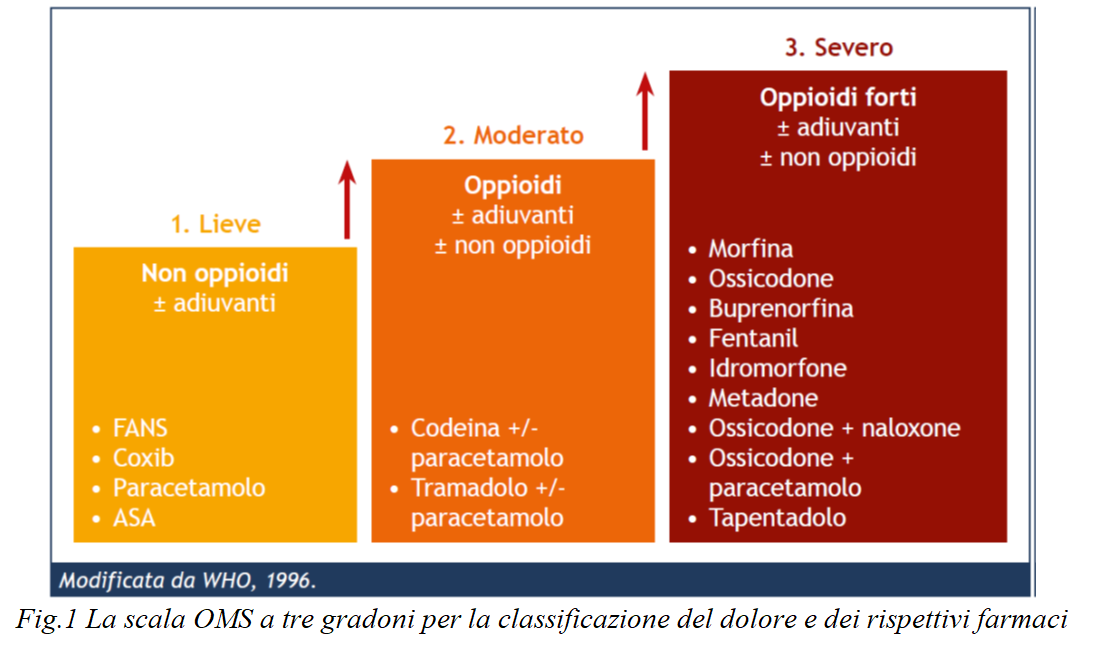
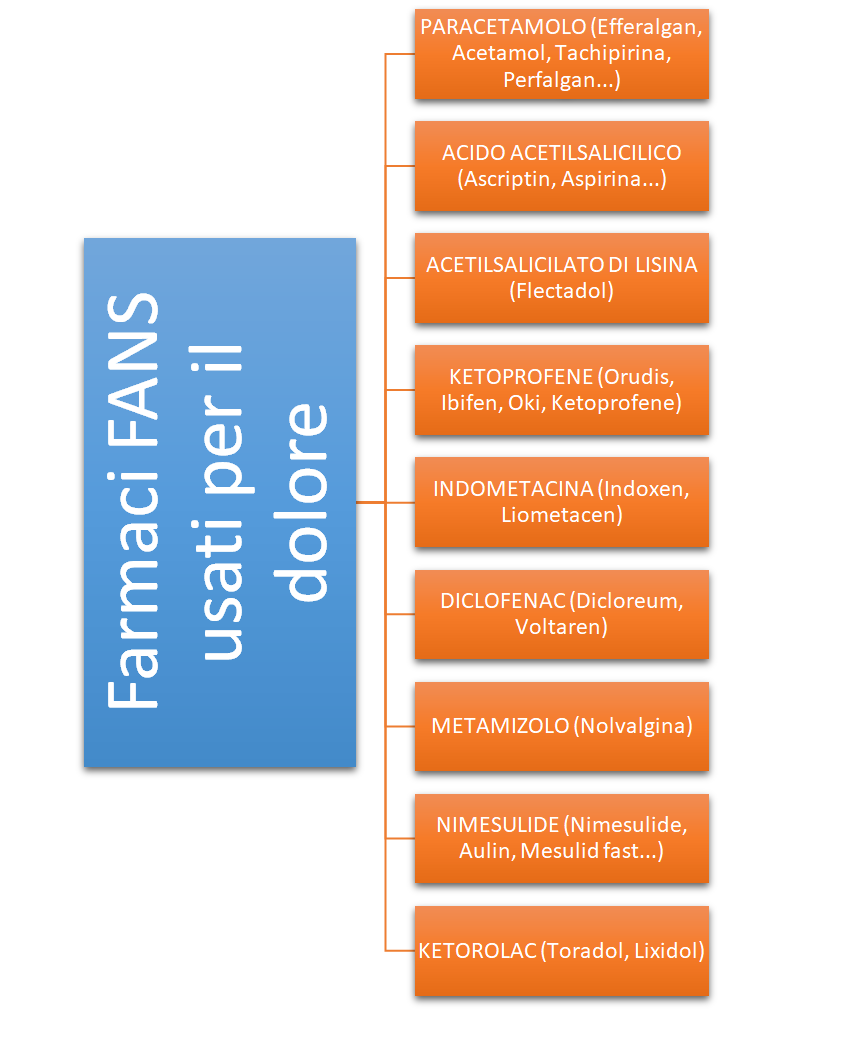
Partendo dal I° STEP, l’attività analgesica dei FANS è correlata all’inibizione dell’enzima ciclossigenasi; le differenze tra i FANS sono modeste, ma vi possono essere diversità nella tolleranza e nella risposta individuale del paziente.
Col tempo sono state introdotte molteplici scale di valutazione per inquadrare al meglio l’intensità del dolore. Abbiamo scale di valutazione unidimensionali (NRS, VAS, VRS, FPS) e multidimensionali (MPQ, BPI, Painad).
- Non utilizzare più di un FANS alla volta
- I FANS sono controindicati in soggetti con ulcera peptica e nello scompenso cardiaco grave
- FANS e Paracetamolo raggiungono tutti un tetto nel loro effetto analgesico all’aumentare della dose
- I FANS e il paracetamolo possono essere somministrati contemporaneamente agli oppioidi per ottenere un effetto analgesico additivo che permette anche l’uso di dosi inferiori di oppioidi.
Gli effetti collaterali di tutti i FANS sono simili qualitativamente a quelli dell’ASA, ad eccezione del rischio di precipitare asma e reazioni anafilattoidi nei pazienti con ipersensibilità all’ASA; una singola dose o poche dosi di FANS orali causano pochi effetti collaterali. Diversamente dall’ASA che ha un effetto irreversibile, i FANS determinano un’inibizione reversibile dell’aggregazione piastrinica per cui la funzione piastrinica riprende quando la maggior parte del farmaco è stata eliminata. Tutti i FANS sono associati a tossicità gastrointestinale grave, anche se il rischio maggiore è per gli anziani, si consiglia pertanto di iniziare con la dose più bassa efficace e di non utilizzare più di un FANS alla volta, ricordando che tutti i FANS sono controindicati nei soggetti con ulcera peptica. L’utilizzo cronico può portare a sanguinamento, ulcerazione e perforazioni fatali con ciascuno di questi farmaci.
I FANS riducono la sintesi delle prostaglandine renali vasodilatatrici, riducono il flusso plasmatici renale, causano ritenzione idrica e possono provocare insufficienza renale in alcuni pazienti. I FANS vanno utilizzati con cautela negli anziani, in pazienti con patologie allergiche, durante la gravidanza, l’allattamento e nei difetti della coagulazione, nei soggetti con insufficienza renale, cardiaca o epatica è anche opportuno somministrare la dose minima possibile controllando la funzionalità renale.
Nel II° STEP s’inizia a parlare invece degli oppiacei deboli.
- PARACETAMOLO + CODEINA (Tachidol, CO-Efferalgan)
L’associazione paracetamolo-codeina possiede una attività antalgica superiore a quella dei suoi componenti presi singolarmente, con un effetto nettamente più prolungato nel tempo. La loro azione è sinergica in quanto il paracetamolo agisce sui meccanismi biochimici centrali e periferici del dolore, mentre la codeina agisce come agonista dei recettori μ degli oppioidi (oppioide debole).
- TRAMADOLO (Fortradol, Contramal)
Analgesico oppioide, agonista dei recettori μ; inibisce la ricaptazione di serotonina e noradrenalina, pertanto produce analgesia con due meccanismi: un effetto oppioidi e un potenziamento delle vie serotoninergiche e adrenergiche. Il tramadolo possiede pochi effetti indesiderati, in particolare dà minore depressione respiratoria, stitichezza e assuefazione; sono state segnalate crisi epilettiche e disturbi psichiatrici.
Infine per l’ultimo STEP, e dunque per il dolore severo, vi sono gli oppiacei forti. Gli oppioidi sono considerati i farmaci di scelta per il dolore acuto grave e per il dolore neoplastico e per il dolore cronico non neoplastico; costituiscono la categoria di farmaci con il più ampio spettro di vie di somministrazione.
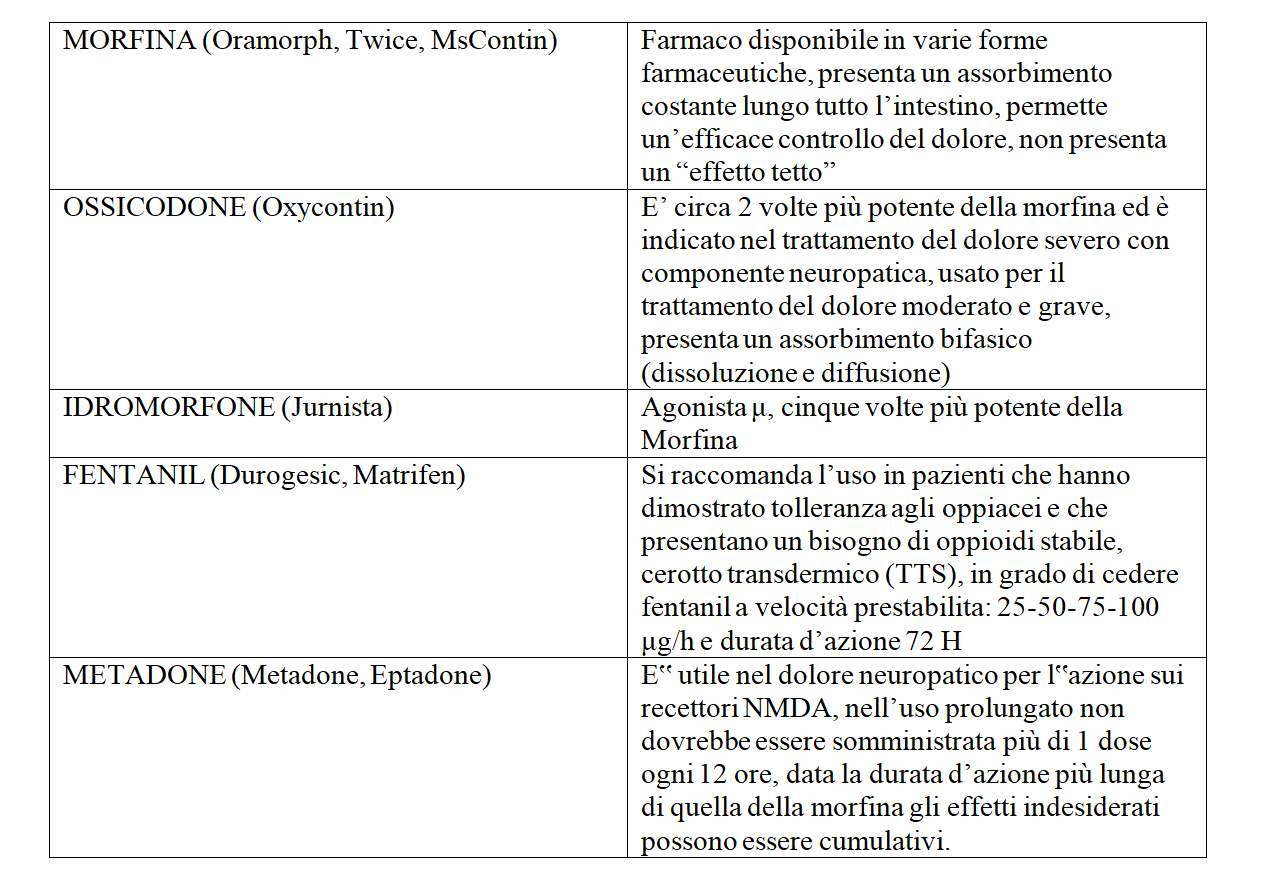
La sedazione indotta dagli oppioidi può essere ridotta diminuendo le dosi e aumentando la frequenza di somministrazione. Generalmente si sviluppa rapidamente una tolleranza nei confronti degli effetti sedativi ed emetici di questi farmaci, ma non della stipsi: un lassativo o un emolliente delle feci dovrebbe essere somministrato precocemente all’inizio del trattamento.
Gli effetti collaterali più comuni degli oppioidi sono sedazione, tossicità cognitiva, allucinazioni, vertigini, nausea, vomito e stipsi; il più grave è la depressione respiratoria.
Tra gli effetti collaterali per l’uso prolungato di oppioidi si segnala la sudorazione e l’iperprolattinemia con diminuzione del testosterone e della fertilità procreativa.
Gli oppioidi, compresi gli agonisti-antagonisti misti, possono inibire il centro del respiro e possono causare apnea in pazienti con broncopneumopatia cronica ostruttiva, cuore polmonare, ridotta riserva respiratoria o preesistente depressione respiratoria, anche alle dosi abituali. I pazienti non affetti da malattie polmonari che assumono oppioidi cronicamente sono spesso tolleranti verso l’effetto di depressione respiratoria, tuttavia l’aggiunta di anestetici generali, fenotiazine, sedativi ipnotici, antidepressivi triciclici o altri depressori del SNC, aumenta questo rischio. Gli effetti collaterali determinati dalla morfina vanno trattati in maniera sistemica con i farmaci adiuvanti e in caso di insuccesso si dovrà passare ad un altro oppiode dello stesso scalino.
Spero che anche questa volta sia stato adeguatamente esaustivo.
Alla prossima colleghi!
Pasquale Fava
- Como, pacemaker senza fili di ultima generazione impiantato all’ospedale Sant’Anna
- Casa circondariale di Ascoli Piceno, raggiunto accordo per l’erogazione del buono pasto agli infermieri. Nursing Up: “Finalmente!”
- Infermieri con titoli esteri in Lombardia, Nursing Up: “Regione chiarisca chi controlla requisiti”
- Demansionamento di 7 infermieri a Taormina: Asp Messina condannata a maxi risarcimento. Esulta il sindacato Nursind
- Uil Fp Lario e Brianza a Bertolaso: “Voucher e incentivi per attrarre infermieri in Lombardia? No, grazie”













Lascia un commento