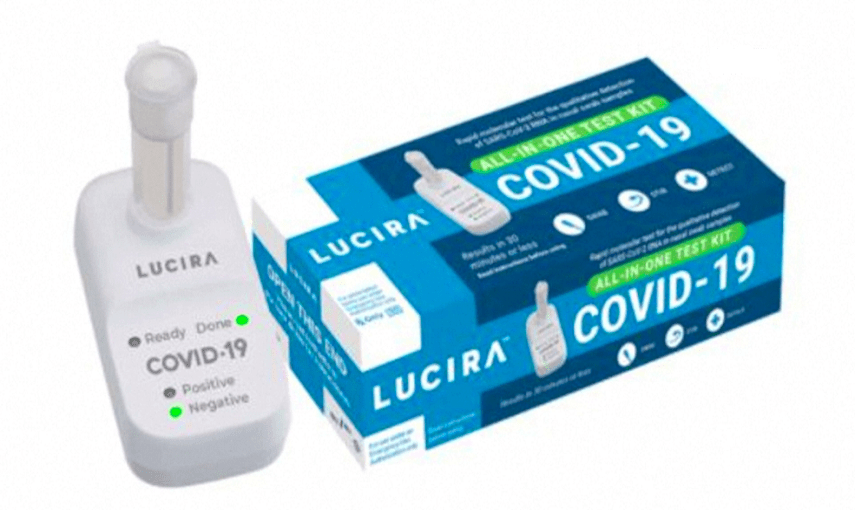
Il kit, prodotto da Lucira Health, fornisce il risultato in soli 30 minuti e attualmente è autorizzato solo per uso su prescrizione.
La statunitense Food and Drug Administration (Fda) ha rilasciato un’autorizzazione all’uso di emergenza (Eua) per il primo test diagnostico auto-test diagnostico a casa che fornisce risultati rapidi sull’eventual infezione da coronavirus: il test molecolare Lucira COVID-19 All-In-One Test Kit.
“La Fda continua a dimostrare la sua velocità senza precedenti in risposta alla pandemia – ha affermato il commissario della Fda, Stephen M. Hahn –. Sebbene i test diagnostici Covid-19 siano stati autorizzati per la raccolta a casa, questo è il primo che può essere completamente auto-somministrato e fornire risultati a casa. Questa nuova opzione di test è un importante progresso diagnostico per affrontare la pandemia e ridurre il carico pubblico della trasmissione della malattia. L’azione odierna sottolinea l’impegno costante della Fda per espandere l’accesso ai test Covid-19 “.
Il test Lucira COVID-19 All-In-One Test Kit è stato autorizzato per l’uso domestico con campioni di tamponi nasali auto-raccolti in soggetti di età pari o superiore a 14 anni sospettati di coronavirus dal proprio medico. È anche autorizzato per l’uso in strutture point-of-care (POC), come ad esempio studi medici, ospedali, centri di assistenza urgente e pronto soccorso) per tutte le età, ma i campioni devono essere raccolti da un operatore sanitario quando il test viene utilizzato presso il POC per testare individui di età inferiore ai 14 anni. Il test è attualmente autorizzato solo per uso su prescrizione.
Il test funziona facendo roteare il tampone del campione auto-raccolto in una fiala, che viene quindi collocata nell’unità di test. In 30 minuti o meno, i risultati possono essere letti direttamente dal display luminoso dell’unità di test che mostra se una persona è positiva o negativa per il SARS-CoV-2. I risultati positivi indicano la presenza del virus. Gli individui con risultati positivi dovrebbero autoisolarsi e cercare cure aggiuntive dal proprio medico. Gli individui che risultano negativi al test e manifestano sintomi simili al Covid-19 dovrebbero seguire il proprio medico curante poiché i risultati negativi non precludono a un individuo l’infezione da SARS-CoV-2.
“L’autorizzazione odierna per un test completo a casa è un passo significativo verso la risposta nazionale della Fda al Covid-19 – ha affermato Jeff Shuren, direttore del Center for Devices and Radiological Health della Fda –. Un test che può essere completamente somministrato interamente al di fuori di un laboratorio o di una struttura sanitaria è sempre stata una delle principali priorità per la Fda per affrontare la pandemia. Ora, più americani che potrebbero avere Covid-19 saranno in grado di intraprendere azioni immediate, in base ai loro risultati, per proteggere se stessi e coloro che li circondano. Non vediamo l’ora di lavorare in modo proattivo con gli sviluppatori di test per supportare la disponibilità di più opzioni di test a casa”.
Una componente importante per il successo dei test a casa è la capacità di tracciare e monitorare in modo efficiente i risultati. Come indicato in questa Eua, gli operatori sanitari prescrittori sono tenuti a riportare tutti i risultati dei test che ricevono dalle persone che utilizzano il test alle autorità sanitarie pubbliche competenti in conformità con i requisiti locali, statali e federali. Lucira Health, il produttore del test, ha anche sviluppato l’etichettatura delle scatole, le istruzioni di riferimento rapido e le istruzioni per gli operatori sanitari al fine di assistere con la segnalazione.
Redazione Nurse Times










Lascia un commento