Di seguito le indicazioni dell’Associazione Italiana di Epidemiologia (AIE) sullo strumento per il controllo dell’epidemia.
Riassunto – L’uso dei test antigenici è proposto ormai come un sostituto del test molecolare in alcune condizioni e le regioni si apprestano all’erogazione massiva. Occorre fare chiarezza sul loro significato ed uso alla luce delle considerazioni delle indicazioni del European Centre for Disease Prevention and Control (ECDC, 2020) che riconosce cinque obiettivi per il loro impiego:
- controllare la trasmissione;
- monitorare le velocità di trasmissione del virus SARS-CoV-2 e la sua gravità;
- mitigare l’impatto del COVID-19 nelle strutture sanitarie e assistenziali;
- rilevare cluster o focolai in situazioni specifiche;
- mantenere lo stato di eliminazione del COVID-19, una volta raggiunto.
Quanto possiamo fidarci dell’esito di un test per mettere in evidenza lo stato di infezione? Questo dipende dalla corrispondenza fra l’esito del test (positivo o negativo) e la realtà di fatto (infezione presente o assente). Nessun test è accurato al cento per cento: ci potranno essere casi di infezione presente per i quali il test risulta negativo (Falso Negativo) e persone sane che risulteranno positive (Falso Positivo). Si tratta di caratteristiche del test note, grazie agli studi di valutazione pre-marketing. In pratica però, la performance del test dipende anche dal contesto in cui viene impiegato: aumenta quando il test è impiegato su persone con elevate probabilità di essere infetti, ad esempio tra i sintomatici al Pronto Soccorso, e si riduce quando impiegato su persone apparentemente sane, ad esempio per uno screening in una scuola oppure in una palestra. Per questo motivo, è fondamentale distinguere se lo scopo primario sia di fare diagnosi su sospetto di malattia (soggetti sintomatici o fortemente a rischio) oppure per la sorveglianza di popolazioni in cui il rischio è comunque aumentato oppure per lo screening su popolazione apparentemente sana.
Tenendo conto della validità dei test e delle possibili finalità e dei possibili usi del test, l’AIE ha prodotto delle raccomandazioni specifiche. In breve:
- Situazioni a maggior rischio in cui è attualmente indicato il test molecolare: si può utilizzare un test rapido che individui subito la positività ed isolare comunque gli individui positivi, ma va eseguito contemporaneamente il test molecolare per tutti i soggetti.
- Situazioni specifiche in cui occorre una sorveglianza perché si sospetta un rischio aumentato: si può utilizzare un test rapido che individui subito la positività ed isolare comunque gli individui positivi, ma va eseguito il test molecolare di conferma per i soggetti positivi.
- Situazioni a basso rischio: l’introduzione di test per screening di massa in situazioni di basso rischio appare prematura e deve tenere conto della bassa validità del test in queste condizioni e soprattutto della compatibilità con le attuali risorse e situazione epidemiologica.
Si deve infine notare che il tampone naso-faringeo è un prelievo biologico con una variabilità operatore-dipendente che può influire in modo rilevante sulla sensibilità del test. Poiché il prelievo è lo stesso sia per il test antigenico che per il molecolare è doveroso garantire verifiche periodiche dell’accuratezza del test, con test di conferma o con doppi prelievi incrociati, analizzati per centri prelievo o per operatore.
Premessa – Mentre il quadro dell’epidemia diventa ogni giorno più preoccupante, si moltiplicano le iniziative ed i suggerimenti per interventi radicali e immediati e si propongono nuove prospettive per superare a lungo termine la minaccia della epidemia. La proposta che trova una valida sponda in ambito internazionale (Peto et al, 2020, Mina et al, 2020) è quella di test rapidi, ripetuti nel tempo, di basso costo da applicare a tutta la popolazione. Allo stato attuale i test rapidi salivari (antigenici o molecolari) sono in fase di valutazione e necessitano informazioni aggiuntive per definirne l‘uso.
A differenza del test PCR molecolare, considerato il gold standard, che rileva il materiale genetico del SARS-CoV-2, i test “rapidi” o antigenici rilevano le molecole sulla superficie del virus. I test antigenici danno risultati in meno di 30 minuti, non devono essere elaborati in laboratorio e sono economici da produrre, sono molto specifici per il virus, ma non sono così sensibili come i test PCR molecolari. L’uso dei test antigenici è proposto ormai come un sostituto del test molecolare in alcune condizioni (Ministero della Salute, Nota tecnica ad interim. Test di laboratorio per SARS-COV-2 e il loro uso in Sanità Pubblica. 16 Ottobre 2020) e le regioni si apprestano all’erogazione massiva. Occorre fare chiarezza sul loro significato ed uso alla luce delle considerazioni del recente documento del WHO (WHO, 2020) e delle indicazioni del European Centre for Disease Prevention and Control (ECDC, 2020) che riconosce cinque obiettivi per il suo impiego in diverse fasi della pandemia:
- controllare la trasmissione;
- monitorare le velocità di trasmissione del virus SARS-CoV-2 e la sua gravità;
- mitigare l’impatto del COVID-19 nelle strutture sanitarie e assistenziali;
- rilevare cluster o focolai in situazioni specifiche;
- mantenere lo stato di eliminazione del COVID-19, una volta raggiunto.
Sensibilità, specificità e valore predittivo del tampone “rapido” – Quanto possiamo fidarci dell’esito di un test per mettere in evidenza lo stato di infezione? Questo dipende dalla corrispondenza fra l’esito del test (positivo o negativo) e la realtà di fatto (infezione presente o assente). Per dare una risposta occorre anzitutto conoscere la sensibilità del test (capacità del test di risultare positivo se applicato a un “infetto”) e la sua specificità (capacità di risultare negativo se applicato a un “non infetto”), entrambe stimate in uno studio di accuratezza diagnostica ben disegnato, condotto e analizzato. Ma non basta. La risposta alla domanda dipende anche da un terzo parametro: dalla prevalenza della condizione indagata, ovvero dalla frequenza degli “infetti” nella popolazione dalla quale il soggetto sottoposto a test è estratto (pre-test probability) (Duca, 2020). Se applicato ad una popolazione, il test avrà un valore predittivo positivo (VPP) (probabilità che una persona con un test positivo sia veramente infetta) e il valore predittivo negativo (VPN) (probabilità che una persona con un test negativo sia veramente non infetta).
La velocità del test antigenico nasofaringeo ha un costo in termini di sensibilità. Mentre un tipico test PCR può rilevare una singola molecola di RNA in un microlitro di soluzione, i test antigenici hanno bisogno di un campione contenente migliaia – probabilmente decine di migliaia – di particelle di virus per microlitro per produrre un risultato positivo. Quindi, se una persona ha basse quantità di virus, il test può dare un risultato falso negativo. Usando come confronto un test PCR standard, uno dei test commerciali ha individuato correttamente il virus nel 95-100% dei casi con campioni raccolti entro una settimana dall’insorgenza dei sintomi. Questa percentuale è scesa al 75% quando i campioni sono stati prelevati più di una settimana dopo che le persone hanno mostrato i primi sintomi. La sensibilità – o il tasso di individuazione delle infezioni – degli altri test antigenici utilizzati negli Stati Uniti è compresa tra l’84% e il 98% (secondo quanto dichiarato dai produttori) se una persona è stata sottoposta al test nella settimana successiva alla comparsa dei sintomi (Guglielmi, 2020).
Il problema della validità del test diagnostico molecolare PCR, e successivamente dei test “rapidi” è stata molto dibattuta durante il corso della pandemia. Il BMJ ha messo a disposizione un calcolatore rapido del valore predittivo positivo e negativo a seconda dei valori di sensibilità e specificità del test (Watson, 2020).
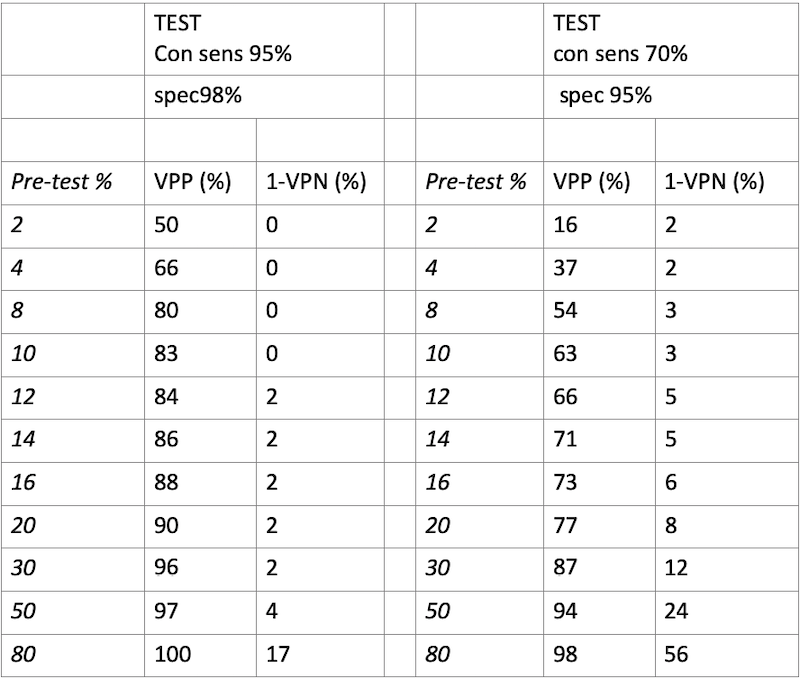
Nella tabella successiva sono indicati i valori di VPP e di 1- VPN (la probabilità che una persona dichiarata sana sia in realtà infetta, falso negativo) a seconda di valori crescenti di prevalenza dell’infezione per due tipi di test, uno con sens 95% e spec 98% e uno con sens 70% e spec 95%. La prima condizione è verosimilmente rappresentata dal test molecolare (PCR) che è il gold standard attuale e i suoi valori relativi di VPP e 1-VPN sono riportati nella prima colonna. Come si può notare anche il test standard non è perfetto, come suggerito da una vasta letteratura sul tema (Watson, 2020). La seconda colonna rappresenta verosimilmente le condizioni del test rapido nasale antigenico. Malgrado i produttori, o chi ha fatto sperimentazione, riportino valori più elevati, occorre tenere presente che si tratta spesso di dichiarazioni basate su dati sperimentali in condizioni ideali (non “sul campo”), verso gold standard non ben definiti, e che non considerano una quota rilevante dell’errore rappresentato dalla modalità di esecuzione del prelievo nasofaringeo. Si noti che 1-VPN è la probabilità di avere l’infezione nonostante il test sia negativo, quindi è la quota di falsi negativi. La tabella viene presentata per un range di valori della prevalenza di infezione (pre-test probability) compresa tra il 2% e l’80%, ovvero in condizioni di aumentato rischio di infezione in comunità (2-4%) e in ambito clinico quando, viceversa, la prevalenza di infezione è molto elevata. Nel caso della seconda colonna (test rapido), i valori del VPP sono relativamente bassi fino a prevalenza del 15% (nel caso di una probabilità a priori del 2% VPP del 16%, fino a un VPP de 73% nel caso di una probabilità a priori del 16%) ad indicare chiaramente la necessità di una conferma dei test positivi quando la prevalenza è bassa.
La probabilità di falsi negativi invece (1-VPN) cresce all’aumentare della prevalenza fino ad essere superiore al 5% nei casi in cui la prevalenza superi quella soglia.
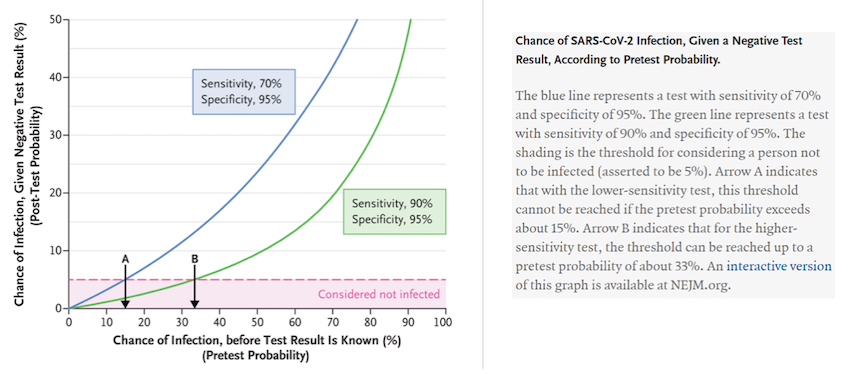
Il tema dei falsi negativi è stato sollevato in un editoriale del NEJM (Woloshin et al, 2020) che ha sottolineato l’importanza della probabilità di infezione pre-test per orientare nella valutazione dei falsi negativi. Questi infatti possono costituire un problema non irrilevante. Il grafico (tratto dallo stesso articolo) fa vedere come a diverse probabilità pre-test si arrivi a frazioni di falsi negativi che possono essere considerati accettabili (in questo caso 5%) o non accettabili.
In sintesi, le conclusioni dello studio sono:
- “I test diagnostici rapidi aiuteranno ma solo se i test saranno altamente sensibili e validati in condizioni realistiche rispetto ad uno standard di riferimento clinicamente significativo”;
- “La FDA dovrebbe garantire che i produttori forniscano i dettagli della sensibilità clinica e della specificità dei test al momento dell’autorizzazione all’immissione in commercio; i test senza tali informazioni avranno meno rilevanza”;
- “La misurazione della sensibilità dei test nelle persone asintomatiche è una priorità urgente. Sarà anche importante sviluppare metodi (ad esempio, regole di previsione) per la stima della probabilità di infezione pre-test (per le persone asintomatiche e sintomatiche) per consentire il calcolo delle probabilità post-test dopo risultati positivi o negativi”;
- “I risultati negativi anche su un test altamente sensibile non possono escludere l’infezione se la probabilità di pre-test è alta, quindi i medici non dovrebbero fidarsi di risultati negativi inaspettati (cioè, supporre che un risultato negativo sia un “falso negativo” in una persona con sintomi tipici ed esposizione nota). È possibile che l’esecuzione di più test simultanei o ripetuti possa superare la limitata sensibilità di un singolo test; tuttavia, tali strategie necessitano di una convalida”.
Possibili ambiti di applicazione del tampone antigenico “rapido”
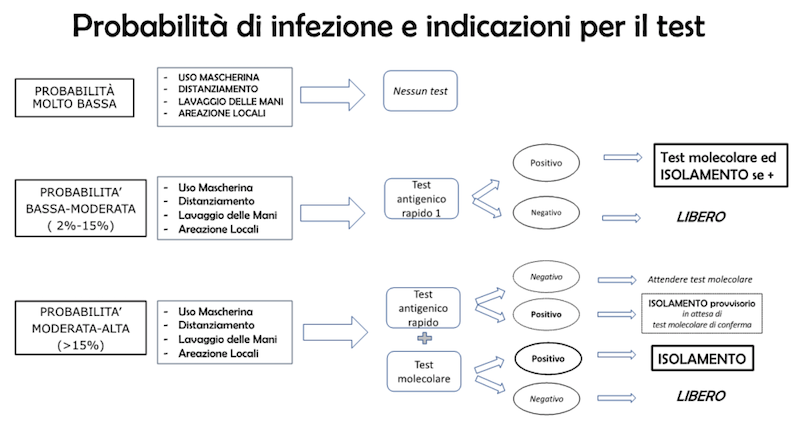
Il tampone nasofaringeo antigenico potrà essere impiegato nei seguenti casi (vedi Figura):
- Quando si effettua l’accertamento di infezioni in soggetti che hanno un’alta probabilità di infezione a priori (del 15% o superiore): test rapido che permette una risposta veloce e l’isolamento immediato dei probabili positivi. Tutti gli esaminati sono da confermare con test molecolare. Si possono ritenere elegibili: pazienti con sintomi di Covid-19 in Pronto Soccorso, persone in focolai accertati, operatori sanitari al lavoro.
Con una probabilità a priori superiore al 15%, con un test a sensibilità del 70% e specificità del 95%, i valori del VPP sono superiori al 73% mentre il tasso di falsi negativi aumenta in modo non accettabile (superiore al 5%). In queste situazioni è raccomandabile effettuare in modo sequenziale prima il test rapido seguito dal test molecolare in tutti i soggetti. Il test rapido permette l’individuazione immediata dei probabili positivi. Il test molecolare è di conferma anche delle negatività. Il vantaggio è un aumento della velocità di isolamento dei pazienti infetti in situazioni in cui vogliamo ridurre al minimo il rischio di trasmissione.
- Quando si effettua l’accertamento di infezioni in soggetti che hanno una probabilità di infezione a priori intermedia (compresa tra il 2% e il 15%): test rapido, seguito da test molecolare di conferma sui positivi, mentre i negativi possono essere dichiarati tali.
Può essere previsto in soggetti asintomatici ma con fattori di rischio, contatti di caso confermato (incluso in ambiente scolastico o lavorativo), soggetti provenienti da paesi a rischio, comunità come scuole, RSA o luoghi di lavoro per la ricerca di persone con infezione in atto, gruppo esteso di persone in una situazione epidemiologica di rischio aumentato (“zone rosse”).
La soglia del 15% della probabilità di infezione a priori (probabilità pre-test) laddove non sia superata, con un test a sensibilità del 70% e specificità del 95%, si traduce in un VPP fino al 71% e un VPN fino al 95% (ovvero un tasso di falsi negativi fino al 5%). In questo caso è dunque raccomandabile l’effettuazione dei un ulteriore accertamento ovvero di un test molecolare ai positivi mentre i negativi possono essere dichiarati tali.
In sintesi, nei casi di valori di probabilità di infezione pre-test compresa tra il 2 e il 15%:
- Test antigenico rapido NEGATIVO: il paziente deve essere considerato NEGATIVO per infezione da SARS-CoV-2.
- Test antigenico rapido POSITIVO: il paziente deve effettuare un test molecolare di controllo.
È possibile l’applicazione di uno screening di popolazione? In tutte le situazioni in cui la probabilità di infezione è non definibile e bassa, consideriamo orientativamente una probabilità inferiore al 2%, si entra nella campo dello scrreing di popolazione o dell’ “universal testing” su cui si è recentemente espressa in un documento anche lo European Centre for Prevention and Disease Control. Si tratta di test a livello di popolazione, o “test di massa”, ovvero l’esecuzione di un elevato volume di test, indipendentemente dal fatto che le persone mostrino o meno i sintomi al fine di identificare presumibili casi con infezione da SARS-CoV-2 confermata poi in laboratorio. I test su tutta la popolazione vengono anche chiamati screening di massa, test universali e screening di popolazione.
L’applicazione di programmi di screening di massa per Covid-19 è, in questa fase, dovrebbe basarsi sulla notevole esperienza maturata in Italia sui programmi di screening di alta qualità per i tumori. I test su persone senza segni o sintomi presentano importanti differenze rispetto ai test che mirano a raggiungere una diagnosi ovvero sono attuati per ragioni di sorveglianza e di ricerca dei casi. In queste situazioni il rapporto con l’operatore di sanità pubblica offre un certo grado di sicurezza, spiegazioni e consenso.
L’editoriale sul BMJ di Raffle et al (2020) presenta alcuni aspetti che dovrebbero essere considerati per situazioni al di fuori di questo contesto:
- I test di massa per Covid-19 possono mirare a trovare persone con infezione attiva che sono asintomatiche o presintomatiche, in modo che la quarantena, la rapida individuazione e il test di contatti ravvicinati possano interrompere la diffusione. Un tale approccio richiede rapidità e chiarezza su ciò che costituisce un caso. I casi sono attualmente definiti come pazienti in cui il test PCR rileva l’RNA virale, attivo o meno. I “casi” includono inevitabilmente le persone con infezioni passate e quelle con infezione attiva che vengono identificate troppo tardi per avere una influenza sulla trasmissione successiva. In sostanza la definizione di caso è ancora in discussione;
- Un buon test in un ambiente diagnostico può essere meno buono se utilizzato per lo screening. Un determinato test ha una sua sensibilità e specificità. Tuttavia, i valori predittivi, come prima indicato, sono influenzati dalla prevalenza dell’infezione nel gruppo sottoposto al test. Tutti i test di massa producono falsi allarmi (falsi positivi) e casi mancati (falsi negativi). I test effettuati da personale non qualificato, l’autotest e la qualità variabile dei kit di test aggravano le imprecisioni. I valori predittivi di un programma di test, relativi alla capacità di identificare le infezioni attive nella pratica reale, sono diversi dalle misure di laboratorio della qualità dei test. Questi valori predittivi “sul campo” devono essere quantificati e spiegati chiaramente.
- Un programma di screening è un programma di un sistema che deve essere ben coordinato, avere una garanzia di qualità per ogni elemento che lo costituisce e deve essere corredato da un sistema informativo che ne garantisce la valutazione. Il sistema deve garantire che i test siano accessibili, affidabili e adatti a tutti i settori della società altrimenti non saranno raggiunti coloro che hanno più bisogno di test. Il servizio sanitario pubblico deve essere coinvolto e assicurare l’appoggio e la continuità nella assistenza. Uno dei requisiti essenziali di un programma di screening è che siano ben definiti tutti i passi successivi e che ne sia valutata l’efficacia.
- È’ necessario disporre di tutte le informazioni rilevanti dell’individuo sottoposto al test (es. occupazione, contatti di casi noti, residenza istituzionale ecc). I dati derivanti dalla applicazione del programma devono essere attentamente raccolti, analizzati e presentati.
- L’offerta del test deve soddisfare standard etici, come ad esempio l’informazione ai partecipanti sullo scopo, i limiti e le incertezze, sulle modalità di uso dei dati e sulle conseguenze dei risultati.
Tutti questi aspetti non sono stati ancora affrontati in Italia e vi è la necessità di definizioni uniformi e di standard coerenti a livello nazionale. Occorre dunque considerare con molta cautela tali aspetti prima dell’introduzione di test di screening di massa.
Conclusioni
- Nell’applicazione di un test di laboratorio di qualsiasi natura è fondamentale distinguere se lo scopo primario sia fare diagnosi su sospetto di malattia (soggetti sintomatici o fortemente a rischio), escludere l’infezione nei contatti, oppure la sorveglianza sanitaria in gruppi o comunità a rischio, ed infine lo screening di popolazione. . Nei primi due casi la probabilità di malattia è alta, negli altri è molto più bassa e pertanto le strategie da adottare devono essere diverse.
- Ogni test è caratterizzato dalla sua sensibilità, la capacità di identificare la malattia nei soggetti malati e dalla sua specificità, la capacità di escludere correttamente i soggetti sani, per cui in una popolazione si deve essere consapevoli che una quota di soggetti malati può risultare negativa al test e una quota di soggetti sani può risultare positiva, perciò falsamente malata. I criteri che rendono preferibili un test rispetto ad un altro dipendono dalle conseguenze di risultati positivi e negativi.
- In un contesto di popolazione un test è in grado di identificare veramente la malattia in funzione di queste due variabili che si combinano con la reale prevalenza di malattia, quindi con una predittività specifica per quella situazione o popolazione (sia positiva, VPP che negativa, VPN). Intuitivamente, a maggiore probabilità a priori di malattia maggiore è la probabilità che un test positivo sia veramente positivo, mentre con una bassa probabilità di malattia è molto più probabile che non lo sia; analogamente per i negativi. Pertanto, un programma di screening di massa, quando la prevalenza è bassa, rischia di fornire un grande numero di falsi positivi con una difficile gestione del sistema sanitario.
- Tali premesse impongono strategie diverse per popolazioni diverse, con l’applicazione di un test diagnostico per i sospetti malati o per soggetti ad alto rischio e di un test di sorveglianza in popolazioni a minor rischio. In attesa della disponibilità di ulteriori test di più semplice somministrazione, la strategia deve tenere conto: della disponibilità e sostenibilità economica del test, della sua sensibilità e specificità, in funzione della probabilità a priori di malattia ma soprattutto dei tempi di risposta. Pertanto in situazioni a maggior rischio in cui è indicato il test molecolare come attuale gold standard può essere utile o farlo precedere da un test rapido che individui subito la positività nella maggior parte dei casi o isolare comunque gli individui in attesa della risposta del test.
- Il tampone naso-faringeo è un prelievo biologico con una variabilità operatore-dipendente che può influire in modo rilevante sulla sensibilità del test. Poiché il prelievo è lo stesso sia per il test antigenico che per il molecolare è doveroso ottimizzarne la sensibilità, garantendo verifiche periodiche, con test di conferma o con doppi prelievi incrociati, o per centri prelievo o per operatore, oppure effettuando di routine due prelievi paralleli o sequenziali da parte di due operatori diversi.
- Il test antigenico “rapido” può utilmente essere introdotto nelle regioni italiane in tutte quelle situazioni in cui, a causa di un rischio aumentato, debba essere eseguita una ricerca rapida dei soggetti positivi. L’uso del test rapido e la gestione del risultato dipende dalla probabilità iniziale che il soggetto sia affetto. Nel caso di una probabilità moderata-alta di infezione (superiore al 15%), il test rapido può essere utile per la individuazione precoce ma va sempre accompagnato dal test molecolare a tutti i soggetti per evitare i falsi negativi. Nel caso di una probabilità moderata di infezione (2-15%) potrà essere condotto il test rapido avendo cura di confermare i positivi con il test molecolare.
- L’introduzione di screening di massa in situazioni di basso rischio deve tenere conto dei limiti evidenziati ma soprattutto della compatibilità con le attuali risorse e situazione epidemiologica.
Redazione Nurse Times












Lascia un commento